Регуляция кроветворения: механизмы и важные факторы
Содержание:
- Регуляция кроветворения
- Гемопоэтические факторы роста
- Особенности процесса образования клеток крови: теории и факты
- Роль витамина В12 в кроветворении
- Особенности дифференцировки гемопоэтических клеток
- Лимфатические узлы
- Комитовани клетки-предшественники
- Костный мозг
- Распространенные болезни крови и кроветворных органов
- История гематологии
- Виды болезней крови
- Тромбоциты, гемостаз
- Что такое гемопоэз и последствия его нарушений
- Гемопоэз у млекопитающих
- Схема и стадии
Регуляция кроветворения
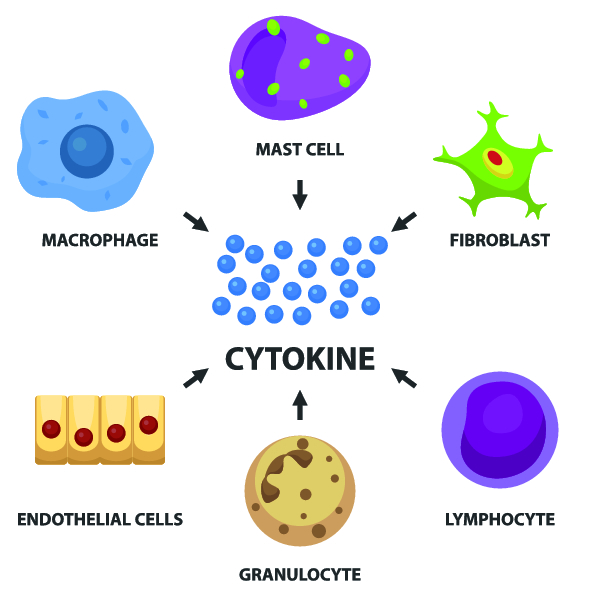 Адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови обеспечивают цитокины.
Адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови обеспечивают цитокины.
В норме регуляция гемопоэза осуществляется непосредственным влиянием микроокружения и гуморальными факторами, обладающими активирующим или угнетающим действием. Эти факторы получили название цитокины. Они позволяют обеспечивать адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови. К цитокинам активирующего типа относятся:
- факторы роста (колониестимулирующие);
- эритропоэтины;
- фактор стволовых клеток;
- интерлейкины и др.
Угнетают клеточную активность и кроветворение следующие субстанции:
- фактор некроза опухоли;
- интерферон-гамма;
- лейкоз-ингибирующий фактор и др.
При этом подавление роста одного вида клеток может приводить к усиленной дифференцировке другого.
Количество клеток в периферической крови регулируется по принципу обратной связи. Так, содержание эритроцитов в крови и насыщение их гемоглобином зависит от потребностей тканей в кислороде. Если она возрастает, то включаются не только компенсаторные механизмы (увеличение частоты дыхания и сердечных сокращений), но и стимулируется эритропоэз.
Гемопоэтические факторы роста
- Гемопоэтические факторы роста (гемоцитокины) — функции, участие в гемопоэзе
- Интерлейкины — виды, функция
- Фактор роста и развития мегакариоцитов (ФРРМ) — строение, функции
- Профилактика нейтропении и ее инфекционных осложнений — рекомендации
- Цитокины в химиотерапии острых нелимфобластных лейкозов — эффективность
- Цитокины в лечении нарушений образования и созревания нейтрофилов — эффективность
- Побочные эффекты Г-КСФ — токсичность филграстима
- Побочные эффекты ГМ-КСФ — токсичность молграмостима
- Дозировки и методы введения Г-КСФ — филграстима, ленограстима
- Дозировки и методы введения ГМ-КСФ — молграмостима, сарграмостим
- Длительность лечения цитокинами (Г-КСФ, ГМ-КСФ) — время начала терапии
- Цитокины (ИЛ-11, агонисты рецепторов Mpl, ФРРМ) в лечении тромбоцитопении — эффективность
- Лечение анемии при опухолях (онкологических заболеваниях) — эффективность эритропоэтина
Особенности процесса образования клеток крови: теории и факты
Процесс образования клеток крови идет непрерывно в течение всей человеческой жизни, интенсивность его строго соответствует потребностям организма.
По одной из современных теорий следует, что клетки крови человека — эритроциты, лейкоциты и тромбоциты происходят из единой родоначальной материнской клетки, так называемой «стволовой». Путем ее деления и развития появляются клепки, предопределяющие различные ветви кроветворения: образование эритроцитов, зернистых лейкоцитов (гранулоцитов), незернистых лейкоцитов (агранулоцитов), тромбоцитов.
Порожденная общей «стволовой» клеткой, каждая из этих ветвей имеет и свою собственную родоначальную клетку. В процессе деления и постепенного созревания и преобразования этих костномозговых элементов появляются зрелые клетки, поступающие в кровь.
К чести русской науки следует оказать, что мысль о происхождении всех клеток крови из единого источника принадлежит знаменитому русскому ученому-гистологу А. А. Максимову, создавшему еще в 1900—1914 гг. свою теорию кроветворения. Эти исследования нашли подтверждение и дальнейшее развитие в трудах советских исследователей.
Вместе с тем в некоторыми учеными высказывалась мысль о том, что еще до рождения человека в кроветворных органах предопределен вид каждой кроветворной линии — гранулоцитарной, эритроцитарной, лимфоцитарной. В пользу такой точки зрения приводятся данные биохимических исследований клеток крови и костного мозга.
Так, советские биохимики П. Ф. Сейц и П. С. Луганова обнаружили, что для определенных линий кроветворных элементов характерен определенный вид энергетического обмена. На основании этих данных они полагали, что и происхождение клеточных форм на каком-то этапе должно быть различным, поскольку характерный тип обмена (как группа крови, резус-фактор), возникший в клетке в начальном периоде ее развития, сохраняется во всех клеточных популяциях (производных данной линии).
Роль витамина В12 в кроветворении
В кроветворении принимают участие различные витамины, среди которых особая роль принадлежит витамину В12, содержащему кобальт.
Источником витамина В12 служат продукты животного происхождения; в растительных продуктах он отсутствует. Благодаря этому витамину поддерживается нормальный процесс созревания эритроцитов у здорового человека.
В сутки взрослому человеку необходимо 3—5 мг витамина В12. Как показали современные исследования, витамин В12, попавший в организм с пищей, всасывается в кишечнике лишь при соединении его с особым белком — гастромукопротеином (который иначе называется «внутренний фактор»).
Гастромукопротеин вырабатывается у человека железами желудка и обладает способностью образовывать с витамином В12 комплексное соединение. Оказалось, что этот белок предохраняет витамин от пожирания микроорганизмами, заселяющими кишечник. Таким образом, он выступает в роли «проводника» витамина В12 и спасает его от разрушающего действия микробов.
Всосавшийся витамин накапливается в печени и затем используется для целей кроветворения по мере необходимости.
Установлено, что витамин B12 принимает активное участие в образовании соединений, являющихся составными частями нуклеиновых кислот, — тех самых кислот, коими так богаты ядра клеток и которые определяют основные наследственные признаки организма.
В случае нехватки витамина B12 задерживается синтез нуклеиновых кислот, в результате чего неизбежно нарушается деление постоянно размножающихся кроветворных клеток. Тогда в костном мозге вместо нормальных эритробластов появляются огромные, медленно созревающие клетки, получившие название мегалобластов (от греческого слова «мегалос» — огромный).
Особенности дифференцировки гемопоэтических клеток
Кроветворная ткань костного мозга объединяет в своем составе комбинацию морфологически нераспознаваемых гемопоэтических клеток-предшественниц и клеток специфических рядов дифференцировки. Все кроветворные клетки, нераспознаваемые с точки зрения морфологии – это гемопоэтические стволовые клетки, которые могут быть:
- мультипотентными (дифференцируются во всех направлениях);
- полипотентными (развиваются только по некоторым из них);
- унипотентными (следуют только по определенному пути развития).
Другая часть клеток, которые удается распознать морфологически, формируется путем дифференцировки из более молодых предшественников, стремительно развивающихся дальше.
Миелопоэз может протекать в нескольких направлениях:
- мегакариоцитарное;
- эритроцитарное;
- моноцитарное;
- гранулоцитарное.
Лимфопоэз включает в себя две основные линии дифференцировки – образование лимфоцитов Т- и В-клеточного ряда. Каждая из них проходит в два этапа. Первый из них является антиген-независимым и заканчивается продукцией структурно зрелых, но иммунологически неактивных лимфоцитов. Следующий этап начинается после контакта с потенциальным антигеном и завершается выработкой специализированных иммунных клеток (Т-киллеров, Т-хелперов, Т-супрессоров, плазматических клеток, клеток памяти).
Каждый ряд дифференцировки кроветворных клеток дебютирует со стадии так называемых «бластов» (например, миелобласты). Для обозначения клеток промежуточного этапа используют приставку «про» и суффикс «цит» (например, проэритрокариоцит). Зрелые клеточные элементы имеют только суффикс «цит» (например, тромбоцит).
Следует отметить, что процесс дифференцировки различных видов клеточных элементов имеет свои особенности. Так, в гранулоцитарном ряде выделяют не одну, а несколько промежуточных стадий. В этом случае вслед за миелобластом образуется промиелоцит, затем миелоцит, метамиелоцит, а только после этого – зрелые клетки – эозинофилы, базофилы, нейтрофилы.
Лимфатические узлы
Лимфоузлы являются периферическим органом кроветворения и важной составляющей частью иммунной системы. Они представляют собой образования овальной или округлой формы, состоящие из сети ретикулярных волокон, между которыми находятся лимфоциты, макрофаги и дендритные клетки
С морфологической точки зрения лимфатический узел можно разделить на три зоны – корковую, субкапсулярную и мозговую:
- В первой из них располагаются В-лимфоциты и макрофаги, образующие первичные фолликулы. После антигенной стимуляции в этой области формируются вторичные фолликулы.
- Субкапсулярная зона заполнена Т-лимфоцитами.
- В медуллярной зоне находятся более зрелые клетки, большинство из которых способны вырабатывать антитела.
Несмотря на то, что лимфоузлы располагаются группами по ходу лимфатических сосудов и рассредоточены по всему организму на значительном расстоянии друг от друга, они тесно взаимосвязаны между собой и выполняют единые функции.
Их формирование заканчивается к 12-15 годам, после 20 лет начинается процесс возрастной инволюции.
Пейеровы бляшки представляют собой скопления лимфоидной ткани по ходу тонкой кишки, их строение аналогично лимфоидным фолликулам лимфатических узлов.
Комитовани клетки-предшественники
На первых этапах кроветворения, мультипотентные стволовые клетки могут дифференцироваться по одному из двух путей, давая начало или клетке-предшественнику лимфоидного ряда, или клеток-предшественников миелоидного ряда. На этот процесс влияет микроокружения, в частности наличие и концентрация определенных факторов роста. Клетки-предшественники лимфоидного или миелоидного ряда отличаются от ГСК своей неспособностью к самовосстановлению, а также тем, что они комитовани к определенному клеточного ряда (то есть их судьба уже определена):
- Комитована клетка-предшественник лимфоидного ряда дает начало Т и В лимфоцитов, а также NK-клеткам (англ. Natural killer cell) и некоторым дендритных клеток;
- Комитована клетка предшественник миелоидного ряда дает начало другим клеткам крови — эритроцитам (красным кровяным тельцам), большинства лейкоцитов (нейтрофилы, эозинофилы, базофилы, моноциты, тучных клеток и дендритные клетки) и мегакариоцитов (от которых отшнуровываются тромбоциты).
Комитування является постепенным процессом. До того, как клетка-предшественник перестанет пролиферировать и станет зрелой, она успевает много раз поделиться и дать начало большому количеству соответствующих специализированных клеток. Из-за этого, в результате всего лишь одного деления ГСК, может образоваться несколько тысяч зрелых клеток различных типов. Именно поэтому ГСК составляют только очень небольшую часть от общей популяции клеток костного мозга. С этой же причине возможно поддерживать высокие темпы кроветворения даже в условиях очень медленного разделения стволовых клеток
А это важно для того, чтобы уменьшить риск возникновения мутаций в стволовых клетках, которое могло бы иметь насидком постоянное образование колоний мутантных клеток в организме. Медленный разделение ГСК также требуется, чтобы избежать репликативного старения
Гемоцитобласты, модифицированные таким образом, что они делятся быстро (например путем нокаута гена Gfi 1, который ограничивает скорость пролиферации) не могут обеспечивать кроветворения в течение всей продолжительности жизни организма.
Костный мозг
В организме человека костный мозг представлен двумя видами – желтым и красным. Последний в постнатальном периоде становится центральным органом гемопоэза. У новорожденного он занимает костно-мозговые полости почти на 100 %. У взрослого человека кроветворная ткань сохраняется преимущественно в центральных отделах скелета (костях черепа и таза, грудной клетки, эпифизах некоторых трубчатых костей).
Собственно кроветворная ткань имеет желеобразную консистенцию и располагается внутри костных трабекул (перегородок) экстраваскулярно, то есть возле сосудов. Сосудистая система играет важную роль в организации костного мозга. Его питание происходит за счет основной питающей артерии и ее ветвей. Кортикальные капилляры проникают в полость костного мозга, образуя разветвленную систему костномозговых синусов, из которых кровь собирается в центральный венозный синус, а затем – в выносящие сосуды.
Желтый костный мозг занимает остальную часть костно-мозговых полостей. Он не активен в отношении кроветворения и состоит из жировой ткани. Однако в условиях сильного гемопоэтического стресса он может превращаться в красный костный мозг.
Распространенные болезни крови и кроветворных органов
Часто встречающаяся патология крови наследственного генеза — это гемофилия. Болезнь обнаруживается в раннем детстве и передается по мужской линии. Из-за дефекта в хромосомах кроветворная система не способна сдерживать начавшееся кровотечение, поэтому при этом заболевании кровопотери могут быть очень обширны.
К распространенным системным болезням крови относиться лейкоз. Это онкологическое заболевание, которое может протекать как в острой, так и в хронической форме. При лейкозе поражается костный мозг, он начинает производить патологические клетки вместо здоровых. Для заболевания характерны лихорадка, боли в костях, выраженный астенический синдром, патологии полости рта (стоматит, гингивит, ангины).
Из аутоиммунных патологий крови нередкими являются тромбоцитопении. Важные структурные элементы крови, тромбоциты, имеют дефекты в строении, из-за этого в клинике этих болезней преобладает склонность к внешним и внутренним кровотечениям, головные и суставные боли, поражения внутренних органов.
История гематологии
- История гематологии: становление, этап развития с 16-го по 19-й век
- История развития теорий кроветворения — второй этап развития гематологии с 19-го по 20-й век
- История клинической гематологии — учения о лейкемиях, лейкозах, лимфомах
- История изучения анемий — второй этап развития гематологии с 19-го по 20-й век
- Третий этап развития гематологии — изучение биологических полимеров (ДНК, белков) клеток крови
- История иммуногематологии — третий этап развития гематологии 20-го по 21-й века
- Отечественные гематологические школы 20-го века. История российской гематологии
- Гематология: История изучения крови
- Концепция единства кровяной ткани. Кровь как мезенхимальная ткань
Виды болезней крови
Многочисленные патологии кроветворения условно объединяют в 3 больших группы:
- анемические, главной характеристикой этих болезней является низкий показатель содержания гемоглобина в крови;
- диатезы геморрагической природы, когда нарушено время свертываемости крови;
- опухолевые процессы, которые могут развиваться в различных органах кроветворения и кровеносной системы.
Выделяют также идиопатические заболевания неустановленной этиологии.
В основе анемий лежат уменьшение количества гемоглобина. Его снижение в крови может быть вызвано нарушением его синтеза (недостаточной выработкой) или патологией в строении эритроцитов, которые доставляют его ко всем системам организма. Также патология может обуславливаться ускоренным распадом гемоглобина или эритроцитов, в этом случае они не успевают выполнить свои функции.
Отдельной группой анемий выступают геморрагические недуги, связанные с кровопотерей. Если человек одномоментно теряет от полу-литра крови — это опасное острое состояние, которое требует безотлагательной медицинской помощи. Длительные кровотечения небольших объемов относят к хроническим, они не так опасны, но без соответствующего лечения приводят к истощению организма.
Патологии, связанные с нарушением продуцирования гемоглобина, часто имеют врожденную природу, но могут возникать и на фоне плохого питания, при снижении в рационе мясных блюд, дефиците микроэлементов (железа, меди, цинка) или витаминов группы В, фолиевой кислоты.
Онкологические заболевания крови характеризуются патологиями крови на клеточном уровне, они делятся на лейкозы (болезни костного мозга) и лимфозы (заболевания лимфатической системы). Если поражается костный мозг, в нем начинают размножаться незрелые атипичные клетки. Онкология лимфоидных сосудов характеризуется нарушениями в клеточной структуре и формированием патологических узлов и уплотнений.
Геморрагические недуги обуславливаются низкой свертываемостью крови из-за снижения количества тромбоцитов, к ним относятся тромбопении, ДВС-синдром, васкулиты.
В классификацию заболеваний крови входят заболевания, которые нельзя отнести ни к одной из групп. Это агранулоцитоз (дефицит эозинофилов, базофилов и нейтрофилов), эозинофилия — усиленное продуцирование эозинофилов, цитостатическая болезнь — недуг, связанный с лечением противоопухолевыми препаратами.
Тромбоциты, гемостаз
- Тромбоциты. Структура тромбоцитов. Функции тромбоцитов. Функции гликопротеинов. Зона золя — геля гиалоплазмы.
- Тромбоцитопоэз. Регуляция тромбоцитопоэза. Тромбопоэтин ( тромбоцитопоэтин ). Мегакариоциты. Тромбоцитопения.
- Гемостаз. Механизмы свертывания крови. Тромбоцитарный гемостаз. Тромбоцитарная реакция. Первичный гемостаз.
- Система свертывания крови. Внешний путь активации свертывания крови. Факторы свертывания крови.
- Внутренний путь активации свертывания крови. Тромбин.
- Противосвертывающая система крови. Противосвертывающие механизмы крови. Антитромбин. Гепарин. Протеины. Простациклин. Тромбомодулин.
- Тканевый активатор плазминогена. Эктоэнзимы. Роль эндотелия в противосвертывающей системе. Тканевый фактор. Ингибитор активатора плазминогена. Фактор Виллебранда. Антикоагулянты.
- Фибринолиз. Плазмин. Антиплазмин. Лизирование ( лизис ) тромба.
- Свойства тромбоцитов. Тромбоцитарная пробка
- Закрытие мелких повреждений в сосудах. Основная теория свертывания крови
- Превращение протромбина в тромбин. Превращение фибриногена в фибрин
- Кровяной сгусток. Механизм формирования сгустков
- Инициация коагуляции. Внешний путь инициации свертывания
- Внутренний путь инициации свертывания. Роль ионов кальция в свертывании
- Суммарная инициация свертывания крови. Внутрисосудистые антикоагулянты
- Лизис кровяных сгустков — плазмин. Повышенная кровоточивость
- Гемофилия и ее причины. Тромбоцитопения и ее причины
- Тромбоэмболические состояния у человека. Причины тромбоэмболий
- Гепарин в виде антикоагулянта. Кумарины
- Оценка состояния свертывания крови. Протромбиновое время (ПТИ)
- Аномалия тромбоцитов Геммелера (Hemmeler) — причины, клиника
а) Патология тромбоцитов
б) Смешанная патология клеток крови
- Аномалии Алиуса-Григнаского (Alius-Grignaschi), Джорданса (Jordans) — причины, клиника
- Аномалия Чедиака-Штейнбринка-Хигаши (Chediak-Steinbrinnk-Higashi) — причины, клиника
- Аномалия Альдера — причины, клиника
- Аномалия Мея-Хегглина (May-Hegglin) — причины, клиника
- Аномалия Пельгера-Хюэта (Pelger-Huet) — причины, клиника
- Цитохимия и биохимия аномалий клеток крови
б) Сосудистые пурпуры
- Сосудистые пурпуры — виды, классификация
- Распространенные поражения сосудов
- Ограниченные поражения сосудистых стенок
- Капилляро-токсическая аллергическая пурпура (болезнь Шенлейн-Геноха) — история изучения
- Клиника болезни Шенлейн-Геноха — симптомы
- Лабораторная диагностика пурпуры Шенлейн-Геноха — анализы
- Механизмы развития болезни Шенлейн-Геноха — патогенез
- Дифференциальная диагностика пурпуры Шенлейн-Геноха
- Неаллергические формы сосудистой пурпуры: цинга, purpura sumplex
- Дисгаммаглобулинемические или гипергаммаглобулинемические пурпуры — механизмы развития
- Лечение болезни Шенлейн-Геноха — сосудистых пурпур
- Геморрагический васкулит — болезнь Шенлейн-Геноха у детей. Причины
- Клиника и диагностика геморрагического васккулита (болезни Шенлейн-Геноха) у детей
- Семейный геморрагический ангиоматоз (болезнь Рендю-Ослера-Вебера)
Что такое гемопоэз и последствия его нарушений
Кроветворение – это очень сложный процесс, он должен постоянно регулироваться и никак не изменяться. Любое изменение в ту или иную сторону приводит к нарушениям в организме и к возникновению различных заболеваний. Гемопоэз, что это такое и с чего он начинается, рассмотрим ниже.
В первые дни жизни эмбриона кроветворение происходит в стенках желчного мешка, в его утолщениях. Начало этого процесса приходится на 16-19 день развития, а после 60-го дня кроветворение начинает происходить в печени, селезенке и в тимусе. Затем, когда развился костный мозг (а он развивается самым последним из кроветворных органов), эти функции переходят к нему. Тогда в печени активное образование крови прекращается.
Как уже упоминалось выше, из стволовых клеток образуются миелоидные клетки (эритроциты, моноциты, тромбоциты, гранулоциты
)
. Этот процесс получил название миелопоэз
. Выработка предшественников лимфоидных клеток – лимфопоэз. Процесс миелопоэза осуществляется в миелоидной ткани, которая находится трубчатых, а также во многих губчатых костях. Во время миелопоэза происходит изменение типа клеток. Например, прежде чем стать тромбоцитами, меняется кариотип полиплоидных мегакариоцитов, а при образовании эритроцитов исчезает ядро у клеток эритробласт.
Селезенка, лимфатические узлы, тимус (вилочковая железа) и костный могз отвечают за протекание лимфопоэза. В лимфоидной ткани происходит образование лимфоцитов, плазмоцитов, а также удаляются клетки и остатки из распада.
При некоторых заболеваниях возникают нарушения в костном мозге, что приводит к нарушению кроветворения. Например, при увеличении количества тромбоцитов становится гуще кровь, что может привести к застою крови в различных органах, замедлению кровотока и образованию тромбов, что является большой опасностью для жизни человека.
Если же клеток крови вырабатывается недостаточно, то симптомы проявляются по мере того, как отмирают нормальные клетки. Самыми «маложивущими» являются гранулоциты, поэтому при их исчезновении организм становится более уязвимым для различных инфекций. Потом начинают убывать эритроциты, что проявляется в тромбоцитопении. Появляется кровоточивость. А при уменьшении количества эритроцитов характерными признаками являются бледность, общая слабость, одышка даже при, казалось бы, небольших нагрузках.
Познания в этой области улучшились только недавно, когда генная инженерия и культивирование клеток достигли нового уровня. Появилась возможность регулировать процесс кроветворения, подходя к этому индивидуально, в зависимости от того, сколько клеток недовырабатывается.
Следите за своим здоровьем! И будет не лишним узнать какие , и как бороться с проблемами такого характера.
Гемопоэз у млекопитающих
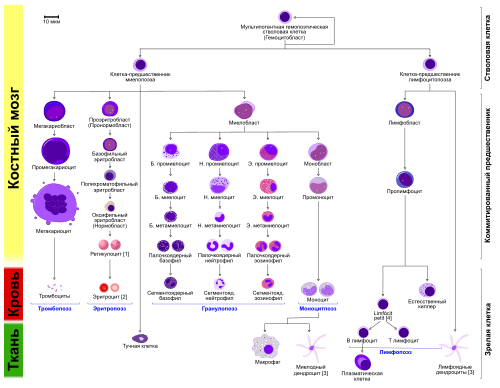
Гемопоэз у человека.
Гемопоэз у млекопитающих осуществляется кроветворными органами, прежде всего — миелоидной тканью красного костного мозга. Некоторая часть лимфоцитов развивается в лимфатических узлах, селезёнке, вилочковой железе (тимусе), которые совместно с красным костным мозгом образуют систему кроветворных органов.
Предшественниками всех клеток — форменных элементов крови являются гемопоэтические стволовые клетки костного мозга, которые могут дифференцироваться двумя путями: в предшественников миелоидных клеток (миелопоэз) и в предшественников лимфоидных клеток (лимфопоэз).
Миелопоэз
При миелопоэзе (др.-греч. μυελός — костный мозг + ποίησις — выработка, образование) в костном мозге образуются форменные элементы крови: эритроциты, гранулоциты, моноциты и тромбоциты. Миелопоэз происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях многих губчатых костей. Ткань, в которой происходит миелопоэз, называется миелоидной. Особенностью миелопоэза человека является изменение кариотипа клеток в процессе дифференциации, так, предшественниками тромбоцитов являются полиплоидные мегакариоциты, а эритробласты при трансформации в эритроциты лишаются ядер.
Лимфопоэз
Лимфопоэз происходит в лимфатических узлах, селезёнке, тимусе и костном мозге. Лимфоидная ткань выполняет несколько основных функций: образование лимфоцитов, образование плазмоцитов и удаление клеток и продуктов их распада.
Эмбриональный гемопоэз млекопитающих
Гемопоэз на эмбриональной стадии претерпевает изменения при онтогенезе. На ранних стадиях развития эмбрионов человека гемопоэз начинается в утолщениях мезодермы желточного мешка, продуцирующего эритроидные клетки примерно с 16—19 дня развития и прекращается после 60-го дня развития, после чего функция кроветворения переходит к печени и селезёнке, начинается лимфопоэз в тимусе (т. н. гепатоспленотимическая стадия). Последним из кроветворных органов в онтогенезе развивается красный костный мозг, играющий главную роль в постэмбриональном гемопоэзе. Костный мозг начинает формироваться в период, когда гематопоэз уже иссяк в желточном мешке, временно осуществляется в печени и активно развивается в тимусе. После окончательного формирования костного мозга гемопоэтическая функция печени угасает.
Схема и стадии
Эритроциты во время своего развития проходят несколько сменяющих друг друга стадий. Гемангиобласт – первичная стволовая клетка, закладывающаяся в онтогенезе. Этот предок всех эндотелиальных и кровеобразующих структур трансформируется в гемоцитобласт – плюрипотентную клетку. Из нее образуется множество различных клеточных элементов, но не целый организм. Мультипотентная стволовая клетка – общий миелоидный предшественник, способный формировать клетки тканей, из которых сам был получен, и превращаться в унипотентную клетку. Она дифференцируется в сторону эритропоэза. Именно с этого звена гемопоэза начинается эритроидная линия.
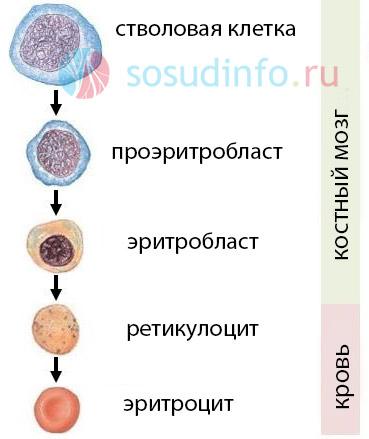
Схема процесса:
- Колониеобразующая единица эритроцитопоэза — лимфоцитоподобная клетка, не имеющая специальных морфологических характеристик, способная к самообновлению и дифференциации.
- Она непрерывно делится и дает начало базофильным клеткам — проэритробластам. Это первый визуально определяемый элемент эритроцитарного ряда, способный к образованию гемоглобина. Его круглое ядро занимает более половины клетки, окрашивается в темно-фиолетовый цвет и имеет тонкодисперсную структуру хроматина.
- В результате его деления образуются базофильные эритробласты. В отличии от своих предшественников они содержат относительно мелкие ядра, базофильную цитоплазму и много рыхлого гетерохроматина.
- Митотическое деление базофильных эритробластов заканчивается появлением полихроматофильных эритробластов, имеющих в ядре конденсированный хроматин.
- Митозы этих клеток дают начало нормобластам, которые прочным кольцом окружают ретикулярную клетку, охватывают ее своими утолщенными отростками и образуют эритробластические островки. Ортохроматические эритробласты не имеют органелл. В их цитоплазме содержится много гемоглобина, а в ядре – глыбок гетерохроматина.
- После выталкивания ядра из тела клетки образуются ретикулоциты. Они синтезируют и накапливают гемоглобин благодаря работе особого рибосомального аппарата. Ретикулоциты выходят из органа кроветворения и попадают в просвет кровеносных сосудов.
- Непосредственно в кровотоке они трансформируются в зрелые эритроцитарные клетки, не имеющие ядра, органелл и рецепторных белков на поверхности. Эритроциты доставляют кислород к органам и удаляют из низ углекислый газ. Процесс созревания длится 24 часа.
Эритроциты на каждой стадии кроветворения имеют особые морфологические, тинкториальные, микроскопические, биохимические и иммунологические свойства. Во время дифференцировки клеток уменьшается размер ядра. Оно постепенно сморщивается и полностью исчезает. Цитоплазма, наоборот, увеличивается в объеме, изменяет свой цвет, накапливает гемоглобин.