Пути выведения лекарственных средств из организма
Содержание:
- Содержание фармакологии.
- Формы лекарственных средств[править | править код]
- Экскреция (выведение) лекарственных средств[править | править код]
- 1.1. Виды физиологических рецепторов
- Математика
- Выведение с мочой[править | править код]
- Распределение лекарственных веществ.
- Как использовать разные формы препарата
- Выведение с мочой
- Другие пути выведения
- Определение биодоступности[править | править код]
- Биодостутность npeпарата
Содержание фармакологии.
Фармакология– это наука о взаимодействии биологических
объектов с химическими веществами.
Взаимодействие
лекарств и организма имеет две стороны:
действие лекарств на организм изучаетфармакодинамика, а действие организма
на лекарства –фармакокинетика.
Фармакодинамика– часть фармакологии, изучающая эффекты
лекарств и механизм их формирования.
Эффектылекарств– это те изменения в функционировании
различных органов и систем организма,
которые развиваются под действием
лекарственных препаратов. Их называют
такжевидами действиялекарств,
а механизмы формирования этих эффектов
–механизмами действия лекарств.
Механизмы действия лекарств можно
рассматривать как их эффекты на различных
уровнях организации живой материи: от
молекулярного до организменного.
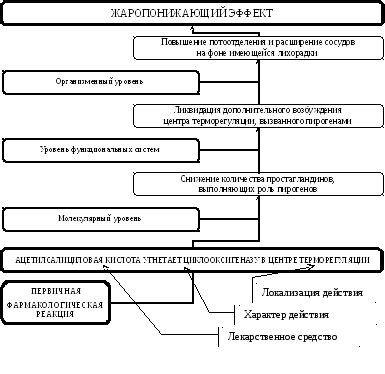
Поясним
данное положение на примере из частной
фармакологии (см. Рис. 1). Ацетилсалициловая
кислота
обладает жаропонижающим эффектом
(организменный уровень). Этот эффект
объясняется повышением потоотделения
и расширением сосудов на фоне имеющейся
лихорадки (это тоже эффекты ацетилсалициловой
кислоты, но их можно рассматривать и
как компонент механизма ее жаропонижающего
действия). Данные эффекты в свою очередь
можно объяснить снятием дополнительного
возбуждения центра терморегуляции,
вызванного пирогенами (мы спускаемся
на уровень функциональных систем). При
желании можно еще более глубоко
погрузиться в тонкости механизма
действия, рассмотрев физиологические
механизмы связи центра терморегуляции
и сосудодвигательного центра,
непосредственно регулирующего тонус
сосудов. Это как взгляд на одну и ту же
структуру через микроскоп с применением
все большего увеличения. Далее (при
переходе на молекулярный уровень) в
данном примере мы увидим снижение
количества простагландинов, выполняющих
в центре терморегуляции роль пирогенов.
Снижение количества простагландинов
в свою очередь объясняется ингибированием
синтезирующего их в условиях воспаления
фермента циклооксигеназы II типа. А
циклооксигеназа – это та молекула, с
которой ацетилсалициловая кислота
непосредственно взаимодействует в
организме (мишень). Обычно с подобной
первичной фармакологической реакции
и начинают изложение любого механизма
любого эффекта любого лекарственного
препарата. Мы сейчас произвели такое
рассмотрение в обратном порядке. Довольно
часто такое подробное объяснение
произвести не удается и отдельные
звенья, а то и целые блоки в механизме
действия лекарств приходится пропускать.
Часто это делается в связи с недостаточной
изученностью, впрочем, в значительном
ряде случаев авторы учебников
подразумевают, что имеют дело с
подготовленными читателями, которые
изучили физиологию, биохимию, общую
фармакологию и смогут самостоятельно
объяснить недостающие звенья механизма
действия.
Рис.
1.
Механизм
действия (схема) на примере жаропонижающего
эффекта ацетилсалициловой кислоты
Таким образом,
фармакодинамика изучает эффекты лекарств
и механизмы их формирования в одном
комплексе. Знание механизмов действия
лекарств позволяет врачу наиболее
рационально использовать фармакотерапию
с учетом индивидуальных особенностей
каждого больного. Именно изучение
механизмов действия является основной
задачей теоретической или экспериментальной
фармакологии.
Фармакокинетика– часть фармакологии, изучающая
всасывание лекарств при различных путях
введения, распределение в организме,
элиминацию (биотрансформацию и выведение),
т.е. их судьбу в организме.
Рис.
2.
Структура
фармакологии (схема)
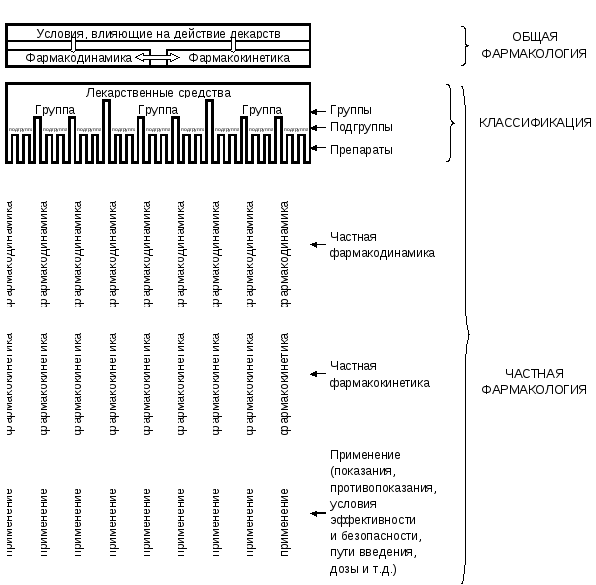 При
При
изучении фармакологии удобно также
выделять такие ее части, как общая и
частная фармакология. Общая фармакологияизучает закономерности взаимодействия
биологических объектов с химическими
веществами, характерные для всех или
многих лекарственных веществ,частная– фармакодинамику и фармакокинетику
отдельных препаратов. Изучение
фармакологии рационально начинать с
общих вопросов, т.к. фармакология
отдельных препаратов подчиняется общим
закономерностям. Следовательно, понимание
общей фармакологии во многом облегчает
изучение частных тем, избавляя от
необходимости заучивания большого
объема материала для каждого препарата.
Формы лекарственных средств[править | править код]
Лекарство вводят (доставляют) в организм в различных формах: в виде таблеток, капсул, растворов, суспензий, препаратов с модифицированным высвобождением, инъецируемых растворов, мазей, кремов, суппозиторий (свечей) и препаратов для ингаляции. Кроме того, лекарственное вещество может представлять собой пролекарство (предшественник активной формы), которое в результате биологических процессов в организме (т.е. метаболизма) превращается в биологически активное вещество.
Таблетка с модифицированным высвобождением. Эта таблетка покрыта мембраной, избирательно проницаемой для воды. Вода поступает внутрь таблетки, и раствор лекарства высвобождается через мелкие отверстия в мембране.
В зависимости от используемой системы доставки лекарственного средства появляется возможность избирательно воздействовать на специфические ткани или избежать системной абсорбции вещества. Таким образом, лекарственная форма и путь введения определяют абсорбцию и распределение. Некоторые формы, например таблетки, капсулы, растворы и суспензии, предназначены для доставки лекарства только через желудочно-кишечный тракт (ЖКТ). Растворы и суспензии применяют внутрь в тех случаях, когда проглатывание таблеток или капсул для пациентов затруднительно.
Способ удлинения времени действия лекарств, которые быстро метаболизируются или экскретируются из организма, состоит в использовании лекарственных форм с контролируемым высвобождением, из которых лекарственное вещество медленно высвобождается во время его прохождения через ЖКТ. Примером системы с контролируемым высвобождением служат таблетки, покрытые полупроницаемой мембраной. С подобной целью можно использовать также другие лекарственные формы, например:
- теофиллин с контролируемым высвобождением для лечения астмы;
- верапамил с контролируемым высвобождением для лечения гипертензии.
Абсорбция лекарства через кожу может оказывать системные эффекты
Система доставки лекарства с помощью накожного пластыря. В этой системе раствор лекарства диффундирует через мембрану, контролирующую количество лекарства, абсорбируемое через кожу.
Пример аппликации лекарства на кожу (пластырь) с целью получения системного эффекта показан на рисунке. Идеальными свойствами препаратов, для которых используют такой тип системы доставки, являются их высокая активность и относительно кратковременная персистенция в организме.
Высокая активность дает возможность применить систему доставки нужного размера, а недолгая персистенция обеспечивает быстрое прекращение действия лекарства, как только система удалена. Например:
накожный пластырь, содержащий скополамин (гиосцин) для предотвращения морской болезни;
накожный пластырь с фентанилом для устранения сильной хронической боли;
накожный пластырь с никотином, используемый лицами с целью отказа от курения.
Апплицируемые лекарства обычно дают местный терапевтический эффект
Лекарства для местного применения используют в виде растворов, мазей, кремов, свечей и аэрозолей. Места их аппликации — глаза, уши, кожа, нос, рот, глотка, легкие, прямая кишка и влагалище. Кожа и слизистые оболочки выполняют барьерную функцию на пути системной абсорбции лекарств.
Экскреция (выведение) лекарственных средств[править | править код]
Лекарственные средства выводятся из организма в неизмененном виде или в виде метаболитов. Полярные соединения экскретируются легче, чем неполярные, жирорастворимые (исключение составляет выведение через легкие), поэтому жирорастворимые препараты сначала превращаются в более полярные метаболиты.
Основной орган, отвечающий за выведение лекарственных средств и их метаболитов, — почки. С калом выводятся невсосавшиеся в кишечнике вещества, а также препараты (и их метаболиты), которые секретируются в желчь или непосредственно в ЖКТ и затем не подвергаются повторному всасыванию. Лекарственные средства, которые выводятся с грудным молоком, могут оказать неблагоприятное действие на ребенка. Легкими выводятся в основном газообразные и летучие соединения и, в очень незначительном количестве, некоторые другие лекарственные средства и их метаболиты.
1.1. Виды физиологических рецепторов
Эффект
большинства лекарственных препаратов
является результатом их взаимодействия
с макромолекулярными компонентами
клеточных мембран. Это взаимодействие
вызывает биохимические и физиологические
изменения, характеризующие эффект
препарата.
Термин
рецептор применяется к клеточной
макромолекуле, с которой препарат
связывается для достижения его эффекта.
Протеины играют важнейшую роль в
формировании рецепторов
Наиболее
важной группой рецепторов для лекарств
являются протеины, физиологически
работают как рецепторы эндогенных
регуляторных лигандов (например,
рецепторы гормонов, нейротрансмиттеров).
Многие лекарства действуют на такие
рецепторы и часто являются высокоселективными
благодаря специфичности физиологических
рецепторов
Регуляторная
активность рецептора может проявляться
как следствие прямого действия на
клеточные мишени, эффекторные протеины,
или через промежуточные клеточные
сигнальные молекулы (трансдуктор).
Взаимодействие рецептора, клеточной
мишени и промежуточных молекул
рассматривают как рецептор-эффекторные
систему.
Рецепторы
связанные с G-протеином.
Большое семейство рецепторов для многих
существующих лекарств (биогенные амины,
эйкозаноиды, пептидные гормоны, опиоиды,
аминокислоты) включает гетеротримерные
регуляторные протеины, связанные с
гуанинтрифосфатом (G-протеины). G-протеины
являются сигнальными трансдукторами,
передающие информацию от рецепторов
эффекторным протеинам, таким как
аденилатциклаза, фосфолипаза С,
фосфодиэстеразы, Са2+
— и К+-ионные
каналы мембрани.
Рецепторы
для ферментов. Группа
рецепторов с внутренней ферментной
активностью включает протеинкиназы
клеточной поверхности, распространяющие
регуляторные сигналы через эффекторные
протеины на внутренней поверхности
клеточной мембраны. Фосфорилирование
протеинов может изменять биохимическую
активность эффектора, или его взаимодействие
с другими протеинами. Большинство
рецепторов, является протеинкиназами,
фосфорилируют тирозин в субстрате. Эта
группа включает рецепторы к инсулину,
факторам роста. Некоторые рецепторные
протеинкиназы фосфорилируют серин и
треонин.
Для
рецепторов, связывающих предсердный
натрийуретический пептид, гуанилин и
урогуанилин, внутриклеточной структурой
является гуанилилциклаза, а не
протеинкиназа. Гуанилилциклаза участвует
в секреции вторичного мессенжера
циклического гуанозинмонофосфата
(ГМФ), активирующего циклическую
ГМФ-зависимую протеинкиназу и активирует
несколько нуклеотидных фосфодиэстераз.
Ионные
каналы.
Рецепторы для некоторых нейротрансмиттеров
формируют селективные ионные каналы.
Эта группа включает никотиновые
холинергические рецепторы, рецепторы
ГАМК, рецепторы для глутамата, аспартата
и глицина.
Рецепторы
регулирующих транскрипцию. Рецепторы
для стероидных и тиреоидных гормонов,
витамина D, ретиноидов — это растворимые
протеины, которые связываются с ДНК и
регулируют транскрипцию специфических
генов.
Большинство
рецепторов в структуре имеют протеины,
их агрегаты и комплексы с нуклеиновыми
кислотами и низкомолекулярными
соединениями.
Математика
В математике элиминация – это изъятие неизвестной величины из системы уравнений. Есть такое понятие в этой науке, как «элиминация кванторов», обозначающее процесс, в результате которого одна заданная логическая формула порождает другую формулу, эквивалентную ей, ту, что свободна от вхождений кванторов.
Когда алгоритм элиминации кванторов возможен, это приносит большую пользу для исследования. Пути нахождения этих алгоритмов для разных теорий имеют нечто общее, поэтому можно говорить о них, как об одном методе. Если удаётся применить данный метод, он оказывается достаточно полезным, поскольку позволяет получить полную информацию об определённой теории. Также он способствует возникновению способа, благодаря которому можно определить, принадлежит то или иное высказывание определённой теории или нет. Другими словами, он доказывает то, что теория разрешаема.
Существуют некоторые теории в математической логике, где допускается элиминация кванторов: теория очередей, алгебра термов, арифметика Пресбургера, плотный линейный порядок, безатомные булевые алгебры.
Таким образом, элиминация кванторов в математике позволяет доказывать теоремы, поскольку порождает способ разрешения определённых задач.
Выведение с мочой[править | править код]
Лекарственные средства могут фильтроваться в почечных клубочках, секретироваться в просвет канальцев и реабсорбироваться из канальцев обратно в плазму. Возрастные изменения функции почек обычно затрагивают эти физиологические процессы в равной степени. У новорожденных функция почек снижена; в течение первых месяцев жизни происходит ее быстрое становление. У пожилых функция почек может быть существенно нарушена, так как в течение жизни она постепенно снижается со скоростью примерно 1% в год.
Количество профильтровавшегося в клубочках лекарственного средства зависит от СКФ и степени связывания препарата с белками плазмы (фильтруется только свободный препарат). В проксимальных почечных канальцах лекарственные средства могут дополнительно секретироваться путем активного транспорта. В роли переносчика амфифильных анионов выступает Р-гликопротеид, а конъюгированных метаболитов (продукты конъюгации с глюкуроновой кислотой, сульфатом и глутатионом) — белок MRP2 (белок полирезистентности-2). Эти переносчики локализуются в мембране щеточной каемки апикальной поверхности эпителиальных клеток.
Сходные системы транспорта органических катионов секретируют препараты, представляющие собой органические основания. Реабсорбируются лекарственные средства главным образом путем неионной диффузии, хотя существуют и системы активного транспорта из просвета канальцев в плазму (эти системы локализуются в основном в дистальных почечных канальцах).
В неионизированной форме слабые кислоты и основания пассивно реабсорбируются в проксимальных и дистальных канальцах по концентрационному градиенту, возникающему благодаря реабсорбции воды. Ионизированные формы слабых электролитов хуже проникают через мембрану эпителиальных клеток канальцев. Таким образом, пассивная реабсорбция слабых электролитов зависит от pH мочи. При ощелачивании мочи слабые кислоты присутствуют в ней преимущественно в ионизированной форме и потому хуже реабсорбируются и в большей степени экскретируются. При закислении мочи, напротив, экскреция слабых кислот снижается. Для слабых оснований ситуация обратная. Ощелачивание и закисление мочи используют при отравлениях некоторыми лекарственными средствами для усиления их почечной экскреции. Степень влияния pH мочи на экскрецию лекарственного средства зависит от выраженности и стойкости изменения pH, а также от того, какой вклад вносит пассивная реабсорбция путем неионной диффузии (см. выше) в элиминацию препарата. Наиболее ощутимо pH мочи влияет на экскрецию слабых кислот и оснований, наполовину диссоциированных при pH от 5 до 8 (то есть в диапазоне колебаний pH мочи). Вместе с тем экскреция и относительно сильных кислот, например салицилатов, возрастает в 4—6 раз при ощелачивании мочи с pH от 6,4 до 8. Доля неионизированных салицилатов при этом уменьшается с 1 до 0,04%.
Распределение лекарственных веществ.
При попадании в кровоток липофильные вещества, как правило, распределяются в организме относительно равномерно, а гидрофильные полярные – неравномерно.
Существенное влияние на характер распределения веществ оказывают биологические барьеры, которые встречаются у них на пути: стенки капилляров, клеточные и плазматические мембраны, гемато-энцефалический и плацентарный барьеры (уместно посмотреть раздел «Фильтрафия через межклеточные промежутки»).
-ГЭБ
Эндотелий капилляров мозга не имеет пор, там практически отсутствует пиноцитоз. Также роль играют астроглии, которые увеличивают барьерную силу.
-гематоофтальмический барьер
Препятствует проникновению гидрофильных полярных веществ из крови в ткань глаза.
-плацентарный
Препятствует проникновению гидрофильных полярных веществ из организма матери в организм плода.
Для характеристики распределения лекарственного вещества в системе однокамерной фармакокинетической модели (организм условно представляется как единое пространство, заполненное жидкостью. При введении лекарственное вещество мгновенно и равномерно распределяется) используют такой показатель как кажущийся объем распределения — Vd
Кажущийся объем распределения отражает предположительный объем жидкости, в котором распределяется вещество.
Если для лекарственного вещества Vd= 3 л (объем плазмы крови), то это означает, что вещество находится в плазме крови, не проникает в форменные элементы крови и невыходит за пределы кровеносного русла. Возможно, это высокомолекулярное вещество (Vd для гепарина = 4 л).
Vd= 15 л означает, что вещество находится в плазме крови (3 л), в межклеточной жидкости (12 л ) и не проникает в клетки тканей. Вероятно, это гидрофильное полярное вещество.
Vd= 400 – 600 – 1000л означает, что ещество депонировано в периферических тканях и его концентрация в крови низкая. Например, для имипрамина – трициклический антидепрессант — Vd= 23л/кг, то есть примерно 1600 л. Это означает, что концентрация имипрамина в крови очень низкая и при отравлении имипрамином гемодиализ неэффективен.
Как использовать разные формы препарата
В лечебных целях Гексикон свечи инструкция по применению предлагает вводить интравагинально, т. е. глубоко во влагалище. Манипуляцию выполняют утром и вечером, используя 1 свечу за 1 раз.

Стандартный курс терапии рассчитан на 7 – 10 суток. По показаниям срок может быть увеличен до 20 дней.
Как профилактическое средство свечи применяют после незащищенного полового акта. Суппозиторий вводят во влагалище в течение первых двух часов с момента окончания сношения. Схема применения Гексикона Д идентична инструкции на свечи 16 мг.
Инструкция

Гель
Гелевая форма Гексикона востребована в терапии воспалительных заболеваний. Пораженные поверхности обрабатывают гелем 2 раза в сутки. Длительность лечения гинекологических и урологических заболеваний – 7 – 10 дней.

Для лечения инфекционных дерматологических патологий гель наносят на проблемные участки 2 – 3 раза в день. Продолжительность лечения зависит от тяжести течения конкретной болезни.
В стоматологии гель используют для наложения аппликаций. Частота процедур – 2 – 3 раза в сутки. Длительность 1 процедуры – 1 – 3 минуты. Продолжительность всего курса определяется клинической ситуацией.
Вагинальные таблетки
Прежде чем ввести таблетку во влагалище, ее смачивают в теплой воде.
Суточная доза в зависимости от диагноза приравнивается к 1 – 2 таблеткам. Курс терапии – 7 – 10 дней. Для профилактики ЗППП вагинальные таблетки, как и гексиконовые свечи, вводят в течение 2 часов по завершению незащищенной половой близости.
Раствор
Раствор для профилактики ИППП целесообразно применять, если процедуру дезинфекции уретрального канала можно запланировать на первые 2 часа после полового акта. Доза раствора для введения в мочеиспускательный канал разная для женщин и мужчин. В первом случае это 1 – 2 мл, во втором – 2 – 3 мл.

Влагалище орошают следующим образом: насадку вводят в орган и впрыскивают 5 – 10 мл вещества. Насадку удерживают 2 – 3 минуты. Также раствором протирают наружные половые органы и кожу лобка и внутренней поверхности бедер. После процедуры не рекомендуется опорожнять мочевой пузырь в течение 2 часов.
При стоматологических заболеваниях раствор Гексикона используют для полосканий ротовой полости. Процедуру выполняют до 4 раз в сутки. На один сеанс берут 5 – 10 мл жидкости.
Противопоказания и побочные эффекты
Единственным противопоказанием к применению свечей и других форм препарата является повышенная чувствительность пациента к компонентам лекарства. В этом случае возникает сильный зуд в области воздействия препарата.
Другими побочными эффектами могут стать:
В случае индивидуальной непереносимости Гексикона врач подбирает эффективные аналоги – Йодоксид, Бетадин, Йодовидон, Макмирор, Повидо-Йод, вагинальные суппозитории с эвкалимином и трихомонацидом.
Выведение с мочой
Лекарственные средства могут фильтроваться в почечных клубочках, секретироваться в просвет канальцев и реабсорбироваться из канальцев обратно в плазму. Возрастные изменения функции почек обычно затрагивают эти физиологические процессы в равной степени. У новорожденных функция почек снижена; в течение первых месяцев жизни происходит ее быстрое становление. У пожилых функция почек может быть существенно нарушена, так как в течение жизни она постепенно снижается со скоростью примерно 1% в год.
Количество профильтровавшегося в клубочках лекарственного средства зависит от СКФ и степени связывания препарата с белками плазмы (фильтруется только свободный препарат). В проксимальных почечных канальцах лекарственные средства могут дополнительно секретироваться путем активного транспорта. В роли переносчика амфифильных анионов выступает Р-гликопротеид, а конъюгированных метаболитов (продукты конъюгации с глюкуроновой кислотой, сульфатом и глутатионом) — белок MRP2 (белок полирезистентности-2). Эти переносчики локализуются в мембране щеточной каемки апикальной поверхности эпителиальных клеток.
Сходные системы транспорта органических катионов секретируют препараты, представляющие собой органические основания. Реабсорбируются лекарственные средства главным образом путем неионной диффузии, хотя существуют и системы активного транспорта из просвета канальцев в плазму (эти системы локализуются в основном в дистальных почечных канальцах).
В неионизированной форме слабые кислоты и основания пассивно реабсорбируются в проксимальных и дистальных канальцах по концентрационному градиенту, возникающему благодаря реабсорбции воды. Ионизированные формы слабых электролитов хуже проникают через мембрану эпителиальных клеток канальцев. Таким образом, пассивная реабсорбция слабых электролитов зависит от pH мочи. При ощелачивании мочи слабые кислоты присутствуют в ней преимущественно в ионизированной форме и потому хуже реабсорбируются и в большей степени экскретируются. При закислении мочи, напротив, экскреция слабых кислот снижается. Для слабых оснований ситуация обратная. Ощелачивание и закисление мочи используют при отравлениях некоторыми лекарственными средствами для усиления их почечной экскреции. Степень влияния pH мочи на экскрецию лекарственного средства зависит от выраженности и стойкости изменения pH, а также от того, какой вклад вносит пассивная реабсорбция путем неионной диффузии (см. выше) в элиминацию препарата. Наиболее ощутимо pH мочи влияет на экскрецию слабых кислот и оснований, наполовину диссоциированных при pH от 5 до 8 (то есть в диапазоне колебаний pH мочи). Вместе с тем экскреция и относительно сильных кислот, например салицилатов, возрастает в 4—6 раз при ощелачивании мочи с pH от 6,4 до 8. Доля неионизированных салицилатов при этом уменьшается с 1 до 0,04%.
Другие пути выведения
Довольно большое количество лекарственного средства может выводиться с потом, со слюной и слезами. Таким путем выводятся в основном неионизированные жирорастворимые препараты, которые проходят через эпителиальные клетки потовых, слюнных и слезных желез путем диффузии. Экскреция слабых электролитов зависит от градиента pH. Лекарственные средства, которые выводятся со слюной, попадают в полость рта и обычно проглатываются. Концентрации некоторых препаратов в слюне и в сыворотке изменяются параллельно друг другу, поэтому в тех случаях, когда получить пробу крови трудно, можно ориентироваться на концентрацию лекарственного средства в слюне. То же самое справедливо и в отношении молока. Поскольку pH молока ниже, чем крови, концентрация основных веществ в молоке может быть чуть выше, чем в крови, а концентрация кислых — наоборот. Неэлектролиты (этанол, мочевина) легко проникают в молоко независимо от pH и достигают в нем той же концентрации, что и в сыворотке. Накопление лекарственных средств в волосах и коже имеет значение для судебно-медицинских исследований.
Определение биодоступности[править | править код]
Обычно биодоступность определяют по количеству лекарственного вещества в крови, то есть величине введенной дозы неизмененного лекарства, которая достигла системного кровообращения, и которая является одной из важнейших фармакокинетических характеристик лекарственного средства. При внутривенном введении биодоступность лекарства составляет 100 %. (Но и при этом биодоступность может быть уменьшена введением другого препарата). Если же данное вещество введено другими путями (например, перорально), то его биодоступность уменьшается, в результате его неполного всасывания и метаболизма, которому это лекарственное средство подвергается в результате первого прохождения.
Биодоступность является также одним из существенных параметров, применяемых в фармакокинетике, учитываемых при расчете режима дозирования для путей введения лекарственных средств, отличающихся от внутривенного. Определяя биодоступность некоторого лекарства, мы характеризуем количество терапевтически активного вещества, которое достигло системного кровотока и стало доступно в месте приложения его действия.
Абсолютная биодоступностьправить | править код
Абсолютная биодоступность — это отношение биодоступности, определенной в виде площади под кривой «концентрация-время» (ППК) активного лекарственного вещества в системном кровотоке после введения путём, иным, чем внутривенный (перорально, ректально, чрезкожно, подкожно), к биодоступности того же самого лекарственного вещества, достигнутой после внутривенного введения. Количество лекарственного вещества, всосавшегося после невнутривенного введения, является лишь долей от того количества лекарства, которое поступило после его внутривенного введения.
Такое сравнение возможно лишь после проведения уподобления доз, если применяли разные дозы для разных путей введения. Из этого следует, что каждую ППК корректируют путём деления соответствующей дозы.
В целях определения величины абсолютной биодоступности некоторого лекарственного вещества проводят фармакокинетическое исследование с целью получения графика «концентрация лекарственного вещества по отношению ко времени» для внутривенного и невнутривенного введения. Другими словами, абсолютная биодоступность — это ППК для откорректированной дозы, когда ППК, полученное для невнутривенного введения, разделено на ППК после внутривенного введения (вв). Формула расчета показателя F для некоторого лекарственного вещества, введенного перорально(по), выглядит следующим образом.
по* ДОЗАвв F= ─────────────── вв* ДОЗАпо
Лекарство, введенное внутривенным путём, имеет величину биодоступности, равную 1 (F=1), тогда как лекарственное вещество, введенное другими путями, имеет величины абсолютной биодоступности меньше единицы.
Относительная биодоступностьправить | править код
Относительная биодоступность — это ППК определенного лекарства, сравнимая с другой рецептурной формой этого же лекарства, принятой за стандарт, или введенной в организм другим путём. Когда стандарт представляет внутривенно введенный препарат, мы имеем дело с абсолютной биодоступностью.
по* ДОЗАвв относительная биодоступность= ─────────────── вв* ДОЗАпо
Для определения относительной биодоступности могут использоваться данные об уровне содержания лекарственного вещества в крови или же его экскреции с мочой после одноразового или многократного введения. Достоверность полученных результатов значительно увеличивается при использовании перекрестного метода исследования, так как при этом устраняются различия, связанные с влиянием физиологического и патологического состояния организма на биодоступность лекарственного вещества.
Биодостутность npeпарата
text_fields
text_fields
arrow_upward
Часть неизмененного лекарства, достигающая системного кровотока после любого способа введения. При внутривенном введении лекарств биодоступность равна 1,0 (100%), при пероралыюм приеме она может значительно уменьшаться (
Следует заметить, что на действие лекарства влияет не только всасываемость, но и скорость всасывания. Вещество с большей скоростью всасывания при равной биодоступности окажет действие раньше и будет дольше сохраняться выше минимальной эффективной концентрации, чем медленно всасывающееся.
У ряда лекарств биодоступность определяется степенью разрушения в печени при первичном прохождении (морфии, бета-адреноблокаторы, пролонгированные нитраты, верапамил, амитриптилин, изониазид и пр.).