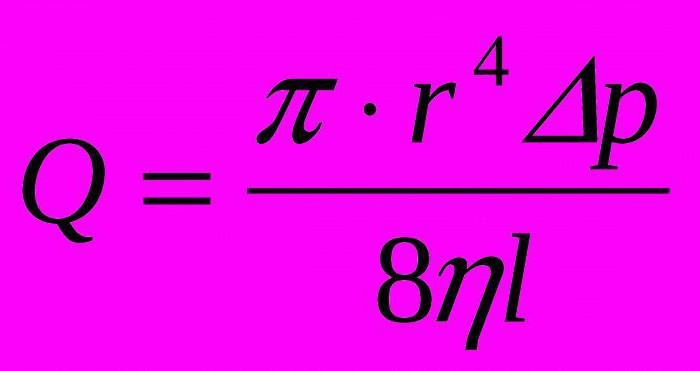Оксиды азота
Содержание:
Оксид азота в бодибилдинге
NО позиционирует себя, как продукт для наращивания мышц, «гемодилятор», который увеличивает размеров мышц, силу, и выносливость. Гемодиляция (hemodilation) означает расширение кровеносных сосудов, ведущих к скелетным мышцам через механизм усиленного притока крови (кровотока). К гемодиляции относят синтез закиси азота. Тот самый человек, который ввел креатин в мир бодибилдинга в 1993 году Эд Берд – основатель EAS, а ныне президент Medical Research Institute (MRI), в настоящее время вводит на рынок спортивного питания оксид азота NО.
Прежде чем принимать оксид азота убедитесь в том, что у вас нет проблем со здоровьем. Примечательно, но данная спортивная добавка, зарекомендовала себя на рынке спортивного питания с лучшей стороны, и она не имеет практически никаких побочных эффектов. Однако, если у вас есть: нарушение свертываемости крови, гемофилия, то для вас, оксид азота является потенциально опасной добавкой, поскольку она увеличивает приток крови, повышает артериальное давление. Поэтому, перед тем, как употреблять NO, рекомендуем вам проконсультироваться с врачом.

Пампинг (накачка) мышц
Побочные эффекты оксида азота на организм
При длительном и не контролируемом приеме донаторов азота, может наблюдаться следующие побочные эффекты:
- головные боли (из-за расширения сосудов мозга)
- рефлекторная тахикардия (ЧСС свыше 90 ударов/минуту, в следствии уменьшения объема крови, циркулирующей в организме человека)
- коллапс (падением кровяного давления и ухудшением кровоснабжения жизненно важных органов)

Действие аргинина
Аргинин используется в человеческом организме для создания всех видов оксида азота, посредством синтеза. Продукты спортивного питания оксида азота, не содержат в свободном виде самого оксида азота, все они содержат различные формы аргинина с использованием A-AKG, которые и являются донаторами оксида азота.
Проводились клинические исследования, и выяснилось, что благодаря молекуле альфакетоглютар (AKG), аргинин лучше сохраняется, не разрушается в желудке, и попадает прямо в кровоток.
Вред оксида азота
Несмотря ни на что, оксиды азота вредны и опасны для человеческого здоровья. Вследствие этого пищевая добавка относится к третьему классу опасности. Например, NO считается сильным ядом, который оказывает влияние на центральную нервную систему, может привести к поражению крови за счет связывания гемоглобина. NO2 также проявляет высокую токсичность, может спровоцировать раздражение дыхательных органов.
Популярные статьи
Читать больше статей
 Ходьба и калории
Ходьба и калории
02.12.2013
Все мы много ходим в течение дня. Даже если у нас малоподвижный образ жизни, мы все равно ходим – ведь у нас н…
612961
65
Подробнее
 Как похудеть в 50 лет
Как похудеть в 50 лет
10.10.2013
Пятьдесят лет для представительниц прекрасного пола – это своеобразный рубеж, перешагнув который каждая вторая…
455396
117
Подробнее
 Бег и калории
Бег и калории
02.12.2013
В наше время бег уже не вызывает массу восторженных отзывов, как это было лет тридцать назад. Тогда общество б…
358513
41
Подробнее
 Гипоаллергенная диета
Гипоаллергенная диета
11.09.2013
Гипоаллергенная диета применяется при всех видах аллергии, независимо от их происхождения, так как позволяет с…
304541
2
Подробнее
 Сбалансированное питание
Сбалансированное питание
19.11.2013
Сбалансированное питание – это то, которое в полной мере и в правильном соотношении обеспечивает поступление в…
250054
8
Подробнее
 Калорийность пирожков
Калорийность пирожков
26.11.2013
Все мы любим пирожки. У многих пирожки – это воспоминания о детстве, о субботнем утре, о деревне; бабушкины пи…
246486
13
Подробнее
Получение
Оксид азота(II) — единственный из оксидов азота, который можно получить непосредственно из свободных элементов соединением азота с кислородом при высоких температурах (1200—1300 °C) или в электрическом разряде. В природе он образуется в атмосфере при грозовых разрядах (тепловой эффект реакции −180,9 кДж):
-
- N2+O2→2NO{\displaystyle {\mathsf {N_{2}+O_{2}\rightarrow 2NO}}}
и тотчас же реагирует с кислородом:
-
- 2NO+O2→2NO2.{\displaystyle {\mathsf {2NO+O_{2}\rightarrow 2NO_{2}.}}}
При понижении температуры оксид азота(II) разлагается на азот и кислород, но если температура падает резко, то не успевший разложиться оксид существует достаточно долго: при низкой температуре скорость распада невелика. Такое резкое охлаждение называется «закалкой» и используется при одном из способов получения азотной кислоты.
В лаборатории его обычно получают взаимодействием 30%-ной HNO3 с некоторыми металлами, например, с медью:
-
- 3Cu+8HNO3→3Cu(NO3)2+2NO+4H2O.{\displaystyle {\mathsf {3Cu+8HNO_{3}\rightarrow 3Cu(NO_{3})_{2}+2NO+4H_{2}O.}}}
Более чистый, не загрязнённый примесями NO можно получить по реакциям:
-
- FeCl2+NaNO2+2HCl→FeCl3+NaCl+NO+H2O,{\displaystyle {\mathsf {FeCl_{2}+NaNO_{2}+2HCl\rightarrow FeCl_{3}+NaCl+NO+H_{2}O,}}}
- 2HNO2+2HI→2NO+I2+2H2O.{\displaystyle {\mathsf {2HNO_{2}+2HI\rightarrow 2NO+I_{2}+2H_{2}O.}}}
Промышленный способ основан на окислении аммиака при высокой температуре и давлении при участии Pt, Cr2O3 (как катализаторов):
-
- 4NH3+5O2→4NO+6H2O.{\displaystyle {\mathsf {4NH_{3}+5O_{2}\rightarrow 4NO+6H_{2}O.}}}
Получение NO является одной из стадий получения азотной кислоты.
Что такое закись азота (веселящий газ)
Закись азота представляет собой оксид азота, имеющий химическую формулу N2О. Название IUPAC для закиси азота оксид азота, Этот газ также называется веселящий газ потому что это вызывает нечувствительность к боли, сопровождаемой легкой истерией, иногда смехом.
Молярная масса этого газа составляет 44 г / моль. Это бесцветный газ при комнатной температуре и давлении. Температура плавления закиси азота составляет -90,86 ° С, а температура кипения составляет -88,48 ° С. Затем2Молекула O состоит из двух атомов азота и атома кислорода. Атомы азота связаны друг с другом, а атом кислорода связан с одним из двух атомов азота. Когда рассматривается химическая связь между этими атомами, N2O показывает резонанс. Есть две основные резонансные структуры для этой молекулы.
Рисунок 3: Резонансные структуры закиси азота
Но фактическая структура является гибридом этих структур.
Рисунок 4: Фактическая структура закиси азота
Закись азота считается инертным газом при комнатной температуре и давлении и имеет очень мало химических реакций. Но когда температура увеличивается, ее реакционная способность также увеличивается. Например, при 187 ° C закись азота реагирует с NaNH2 производство азида натрия (NaN3).
Степень окисления азота в закиси азота составляет +1. Степень окисления кислорода составляет -2, а молекула закиси азота является нейтральным соединением. Тогда степень окисления обоих атомов азота должна быть +2, чтобы сбалансировать уравнение.
Степень окисления закиси азота = 0
Степень окисления атома кислорода = -2
Следовательно,
N2O = 2 (N) + (O)0 = 2 (Н) + (-2)2 (N) = +2(N) = +1
Биологическое значение
Закись азота образуется как при ферментативном, так и при неферментативном восстановлении из окиси азота (II). В опытах in vitro было обнаружено, что закись азота образуется при реакции между окисью азота (II) и тиолом или тиол-содержащими соединениями. Сообщается, что образование N2O из окиси азота было обнаружено в цитозоле гепатоцитов, что заставляет предполагать возможное образование этого газа в клетках млекопитающих в физиологических условиях. В организме бактерий закись азота образуется в ходе процесса, называемого денитрификацией, и катализируемого нитрооксид-редуктазой. Ранее этот процесс предполагался специфичным для некоторых видов бактерий и отсутствующим у млекопитающих, но новые данные заставляют предполагать, что это не так. Было показано, что физиологически релевантные концентрации закиси азота ингибируют как ионные токи, так и опосредуемые эксайтотоксичностью нейродегенеративные процессы, происходящие при чрезмерном возбуждении NMDA-рецепторов. Также закись азота ингибирует биосинтез метионина, угнетая активность метионин-синтетазы и скорость превращения гомоцистеина в метионин и повышая концентрацию гомоцистеина в культурах лимфоцитов и в биоптатах человеческой печени. Хотя закись азота не является лигандом для гема, и не реагирует с тиоловыми группами, она обнаруживается во внутренних структурах гемосодержащих белков, таких, как гемоглобин, миоглобин, цитохромоксидаза. Способность закиси азота нековалентно, обратимо изменять структуру и функции гемосодержащих белков была показана исследованием сдвига инфракрасных спектров тиоловых групп цистеинов гемоглобина и тем, что закись азота способна частично и обратимо ингибировать функцию цитохромоксидазы C. Точные механизмы этого нековалентного взаимодействия закиси азота с гемосодержащими белками и биологическое значение этого явления заслуживают дальнейших исследований. В настоящее время представляется возможным, что эндогенная закись азота участвует в регуляции активности NMDA и опиоидной системы. Обладает нейротоксическими свойствами.
Общее описание
Азот – это бесцветный двухатомный газ (N2). Атомы в молекуле азота удерживает прочная тройная связь, что обуславливает инертность элемента. Азот реагирует с другими элементами и соединениями под действием внешних факторов – высокой температуры, электричества, катализаторов.
Рис. 1. Строение молекулы азота.
Оксиды образуются из солей аммония и азотной кислоты. Формулы оксидов азота и краткая характеристика соединений приведены в таблице.
|
Название |
Формула |
Получение |
Особенности |
|
Оксид диазота или оксид азота (I) – «веселящий газ» |
N2O |
– Нагревание нитрата аммония (опасность взрыва): NH4NO3 → N2O + 2H2O; – нагревание аминосульфоновой кислоты с разбавленной азотной кислотой: NH2SO2OH + HNO3 → N2O + H2SO4 + H2O |
Бесцветный газ со сладковатым привкусом. Не горит, токсичен. Растворим в воде, серной кислота, спирте |
|
Монооксид или оксид азота (II) |
NO |
Единственный оксид, получаемый непосредственным взаимодействием кислорода и азота при температуре 1200°С или при электрических разрядах: N2 + O2 → 2NO |
Бесцветный ядовитый газ. На воздухе окисляется, приобретая коричневый цвет. Трудно сжижается. В жидком виде имеет голубой цвет |
|
Триоксид диазота или оксид азота (III) |
N2O3 |
При взаимодействии разбавленной азотной кислоты и твёрдого оксида мышьяка с последующим охлаждением: – 2HNO3 + As2O3 → NO2 + NO + 2HAsO3; – NO2 + NO → N2O3 |
При нормальных условиях – синяя жидкость. Может приобретать газообразное и твёрдое состояния. Сильно токсичен, вызывает ожоги кожи |
|
Диоксид или оксид азота (IV) |
NO2 |
– При взаимодействии азотной кислоты и меди: Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O; – при разложении нитрата свинца: 2Pb(NO3)2 → 2PbO + 4NO2 + O2 |
Ядовитый газ бурого цвета с острым запахом. Легко сжижается при температуре ниже +21°С, превращаясь в желтоватую жидкость |
|
Пентаоксид диазота или оксид азота (V) |
N2O5 |
– Дегидратация азотной кислоты в присутствии оксида фосфора: 2HNO3 + P2O5 → 2HPO3 + N2O5; – взаимодействие хлора и нитрата серебра: 4AgNO3 + 2Cl2 → 4AgCl + 2N2O5 + O2; – реакция оксида азота (IV) и озона: 2NO2 + O3 → N2O5 + O2 |
Бесцветное твёрдое кристаллическое соединение, крайне неустойчивое при нормальных условиях. Приобретает стабильную форму при температуре ниже +10°C |

Рис. 2. Диоксид или оксид азота (IV).
Помимо пяти стабильных оксидов азота известны ещё пять нестабильных соединений – NON3, NO2N3, N(NO2)3, нитратный радикал NO3 и димер, состоящий из двух простых молекул, диоксида азота (N2O4).
Так на что же влияет усиленное производство NO?
После перегрузки мышц у крыс через некоторое время начинаются процессы их гипертрофии, но если блокировать производство оксида азота, то такой отклик подавляется. У крыс, тренировавшихся и получавших плацебо, размеры целевой мышцы увеличивались через две недели на 76%. (2) Грызуны, получавшие б локатор NO, демонстрировали рост мышечных размеров лишь на уровне 39%.
Очевидно, что не только оксид азота несет ответственность за гипертрофию в ответ на физические нагрузки (поскольку его подавление все же не остановило рост полностью). Однако результаты исследований ясно показали его основное влияние на процессы построения мышц, поскольку подавление NO тормозит рост почти на 50%. Это значит, что для обеспечения максимального анаболизма вы должны оптимизировать производство оксида азота.
С чем же связано то, что NO может оказывать столь значительный эффект роста? Последние исследования объясняют магические анаболические свойства этого вещества.
Биологическое действие:
При применении в хирургической практике, при вдыхании закиси азота очень быстро, через 1-2 минуты, происходит потеря сознания и исчезает болевая чувствительность; наркоз наступает без стадии возбуждения; раздражения слизистых оболочек дыхательных путей не бывает. Сколько-нибудь продолжительное вдыхание чистой закиси азота невозможно, так как она не способна поддерживать дыхание и развивается асфиксия (удушье). Используются ее смеси с кислородом N2O : O2: 80:20 — неполная анальгезия, 86:14 — полная анальгезия, 89:11 — неполный наркоз, 94:6 — полный наркоз.
В крови закись азота находится в растворенном состоянии и в соединение с гемоглобином не вступает. Дыхание под влиянием закиси азота вначале несколько замедляется, а затем ускоряется; пульс слегка учащается, кровяное давление не изменяется, зрачки суживаются, их реакция на свет сохраняется, движения глаз также сохраняются.
Пробуждение после вдыхания закиси азота наступает сразу после прекращения поступления газа в организм. Последствий обычно не бывает. Выделяется закись азота через легкие в неизменном виде.
Влияние на организм оксида азота NО
Оксид азота, представляет собой бесцветный газ, без запаха, легко растворим в воде. Процесс производства оксида азота в организме происходит следующим образом: аргинин, переносит азот к энзимам (ферментам), а те в свою очередь производят оксид азота. Проводились исследования, в которых, было установлено, что относительно высокие концентрации оксида азота в короткий промежуток времени, не вызывают никаких побочных эффектов.
Основные функции оксида азота в организме
Спортивные добавки донаторы оксида азота NО помогают создавать и поддерживать высокий уровень оксида азота в организме
Все знают, что протеин, важно принять сразу после тренировки. Это отчасти так, потому, что оксид азота выступает в роли молекулы, которая сигнализирует ДНК, на увеличение мышечных клеток, мышечных волокон
Путем создания и поддержания высокого уровня NО, вы увеличиваете потенциально, время пикового мышечного роста, с 1-2 часа, до 10-12 часов в сутки.
Производители, рекомендуют снизить потребление глютамина при приеме данной спортивной добавки, потому что глютамин снижает эффективность оксида азота NO.
Действия NO на организм
Правильный прием оксид азота может помочь вам увеличить мышечную массу и силу. Одни атлеты отмечают, что их восстановление происходит быстрее, другие говорят, что оксид азота влияет на силовые показатели, например, один парень увеличил результат в приседаниях со 140 кг до 180 кг, буквально за 5-6 месяцев. Некоторые спортсмены говорят также, о других преимуществах приема оксида азота, таких как, улучшение аппетита, проявление венозности, улучшение интимной жизни и др. Однако, большинство атлетов, не заметили ни каких значительных изменений, которые бы повлияли на рост мышц, увеличение силы, и улучшение концентрации.
Производители заявляют, что прием NO обеспечит огромный прирост мышечной массы, незабываемый мышечный памп на тренировке, полное восстановления организма, и увеличение силовых показателей. Оксид азота, был обнаружен лишь в 1980-е годы, по словам его производителей, MRI, с помощью него, можно понять, почему останавливается мышечный рост.
MRI потребовалось четыре года, чтобы придумать систему доставки и управления активностью NО. Эта система доставки называется «pHyser3«, она заставляет постоянно производить оксид азота, чтобы обеспечивать памп, накачку мышц.

Влияние NO на кровеносный сосуд
Не стоит всему верить, во все что написано про оксид азота NО. Он может действовать по разному, на разных людей, кому то он поможет увеличить силу, и мышечную массу, а кто-то вообще ничего не почувствует. В любом случае, не ожидайте, что он вас превратит в атлета с минимальным количеством жира, и большой мышечной массой. Он расширит ваши сосуды, приток крови в мышцы увеличится, но это не сделает вас невероятным халком.
Однозначно стоит купить, поэкспериментируйте в течение месяца, и посмотрите, пронаблюдайте над собой, своими результатами в тренажерном зале. Покупайте всегда у производителей проверенных временем, которые на рынке спортивного питания зарекомендовали себя с хорошей стороны, опасайтесь подделок. Если качественный оксид азота на ваш организм не действует, то не стоит в следующий раз его покупать.
Что такое веселящий газ, или закись азота?
Веселящим газом называют диоксид диазота, или закись азота. Его химическая формула – N2O. Это бесцветный негорючий газ с характерным сладковатым запахом и привкусом. При нулевой температуре и давлении 30 атмосфер, а также при обычной температуре и давлении 40 атмосфер может сгущаться в бесцветную жидкость. Из одного грамма жидкой закиси азота можно получить пол-литра газа.
Закись азота получают нагреванием сухого нитрата аммония. Делать это в кустарных условиях очень опасно, поскольку при высоких температурах есть вероятность взрыва. Более удобен способ с нагреванием сульфаминовой кислоты с 73%-й азотной кислотой.
Веселящим этот газ прозвал английский химик Хэмфри Дэви, изучавший в 1799 году на себе его свойства. В начальной фазе действия N2O ученый заметил возбуждение, сопровождавшееся смехом и беспорядочными телодвижениями, а в последующей – потерю сознания.
Химические свойства
Кислотный оксид. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель:
-
- 2NO2+2C→2CO2+N2{\displaystyle {\mathsf {2NO_{2}+2C\rightarrow 2CO_{2}+N_{2}}}}
- 10NO2+8P→4P2O5+5N2{\displaystyle {\mathsf {10NO_{2}+8P\rightarrow 4P_{2}O_{5}+5N_{2}}}}
Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты:
-
- SO2+NO2→SO3+NO{\displaystyle {\mathsf {SO_{2}+NO_{2}\rightarrow SO_{3}+NO}}}
При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования):
-
- 2NO2+H2O→HNO3+HNO2{\displaystyle {\mathsf {2NO_{2}+H_{2}O\rightarrow HNO_{3}+HNO_{2}}}}
Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO:
-
- 3NO2+H2O→2HNO3+NO↑{\displaystyle {\mathsf {3NO_{2}+H_{2}O\rightarrow 2HNO_{3}+NO\uparrow }}}
Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя):
-
- 4NO2+2H2O+O2→4HNO3{\displaystyle {\mathsf {4NO_{2}+2H_{2}O+O_{2}\rightarrow 4HNO_{3}}}}
При растворении NO2 в щелочах образуются как нитраты, так и нитриты:
-
- 2NO2+2KOH→KNO3+KNO2+H2O{\displaystyle {\mathsf {2NO_{2}+2KOH\rightarrow KNO_{3}+KNO_{2}+H_{2}O}}}
Жидкий NO2 применяется для получения безводных нитратов:
-
- Zn+2N2O4→Zn(NO3)2+2NO{\displaystyle {\mathsf {Zn+2N_{2}O_{4}\rightarrow Zn(NO_{3})_{2}+2NO}}}
В реакциях с галогенами образует соли нитрония, нитрозила и оксиды галогенов
-
- 2NO2+2Cl2→NOCl+NO2Cl+Cl2O↑{\displaystyle {\mathsf {2NO_{2}+2Cl_{2}\rightarrow NOCl+NO_{2}Cl+Cl_{2}O\uparrow }}}
Лучшие спортивные добавки оксида азота
NO-Xplode (BSN)
Как правило, в бодибилдинге, в основном лучшие добавки, которые используют для выработки организмом оксида азота: аргинин, агматин, экстракт свеклы и некоторые, предтренировочные комплексы, и другие спортивные добавки, например:
- NO-Xplode (BSN)
- V-12 Magnum (SAN)
- naNO Vapor Performance Series (MuscleTech)
- SuperPump 250 (Gaspari Nutrition)
- Xtreme Napalm
- JetFuse NOX GAT
- NO Shotgun (VPX)
- NO2 Platinum (MRI)
В медицинских целях, используют препараты нитроглицерин (глицерилтринитрат) и изосорбида динитрат, молсидомин, нитропруссид натрия, которые отлично справляются с задачей расслабления стенок сосудов, за счет NO.
Примечания
- ↑
- Roszer, T (2012) The Biology of Subcellular Nitric Oxide. ISBN 978-94-007-2818-9
- Stryer, Lubert. Biochemistry, 4th Edition. — W.H. Freeman and Company, 1995. — P. 732. — ISBN 0-7167-2009-4.
- Gorczyniski and Stanely, Clinical Immunology. Landes Bioscience; Austin, TX. ISBN 1-57059-625-5
-
Free text.
- free text
- Janeway, C. A. Immunobiology: the immune system in health and disease. — 6th. — New York : Garland Science, 2005. — ISBN 0-8153-4101-6.
- van Faassen, E. and Vanin, A. (eds.) (2007) Radicals for life: The various forms of nitric oxide. Elsevier, Amsterdam, ISBN 978-0-444-52236-8
- van Faassen, E. and Vanin, A. (2004) «Nitric Oxide», in Encyclopedia of Analytical Science, 2nd ed., Elsevier, ISBN 0-12-764100-9.
- Rhoades, RA. Medical physiology 2nd edition / RA Rhoades, Tanner. — 2003.
Примечания
- ↑
- Roszer, T (2012) The Biology of Subcellular Nitric Oxide. ISBN 978-94-007-2818-9
- Stryer, Lubert. Biochemistry, 4th Edition. — W.H. Freeman and Company, 1995. — P. 732. — ISBN 0-7167-2009-4.
- Gorczyniski and Stanely, Clinical Immunology. Landes Bioscience; Austin, TX. ISBN 1-57059-625-5
-
Free text.
- free text
- Janeway, C. A. Immunobiology: the immune system in health and disease. — 6th. — New York : Garland Science, 2005. — ISBN 0-8153-4101-6.
- van Faassen, E. and Vanin, A. (eds.) (2007) Radicals for life: The various forms of nitric oxide. Elsevier, Amsterdam, ISBN 978-0-444-52236-8
- van Faassen, E. and Vanin, A. (2004) «Nitric Oxide», in Encyclopedia of Analytical Science, 2nd ed., Elsevier, ISBN 0-12-764100-9.
- Rhoades, RA. Medical physiology 2nd edition / RA Rhoades, Tanner. — 2003.
Окись азота в бодибилдинге
Оксид азота создает эффект накачки и надутости мышц за счет притока крови. Считается, что такое кровоснабжение позволяет улучшить гипертрофию мышц, а также ускорить их восстановление. Но на практике результаты исследований очень противоречивы. Так, в некоторых исследованиях добавка позволила получить лишь временный эффект накачки мышц, но к концу эксперимента группа культуристов, употреблявших добавку, и группа, принимавшая плацебо, показали одинаковые результаты в гипертрофии мышц. Хотя первой группе удалось показать лучшие силовые показатели.
Возможно, некоторые противоречивые результаты в исследованиях связаны с тем, что спортивное питание
для повышения выработки окиси азота может стимулировать как анаболические, так и катаболические процессы, поэтому употребление разного объема добавки может иметь абсолютно разные результаты. Вероятно, что употребление большего количества добавки наоборот ослабит эффект, а вовсе не улучшит.
В настоящее время существует множество вариантов спортивного питания, имеющих абривиатуру NO2. Основным стимулятором для повышенной выработки окиси азота в настоящий момент остается аминокислота L-аргинин. Мнение о том, что вы принимаете оксид азота в корне не верно, вы принимаете лишь добавку, которая стимулирует выработку окиси. В чистом виде оксид азота токсичный газ, который при вдыхании может вызвать состояние опьянения и потерю сознания.
Оксид азота помогает расти
Мышечный рост контролируется анаболическими и катаболическими гормонами, а также различными факторами роста. Будучи бодибилдером, вы стремитесь оптимизировать анаболическую среду в собственном организме, увеличивая секрецию анаболических медиаторов и уменьшая высвобождение катаболических гормонов. Однако это легче сказать, чем сделать, поскольку контроль эндокринной системы — это довольно сложный процесс. С другой стороны, оказывается, что контролировать высвобождение оксида азота (NO) не так уж трудно.