Ацетилхолин
Содержание:
- Холинэстераза
- Дефицит ацетилхолина
- Историческая справка
- Взаимодействие холинэстеразы с ингибиторами и реактиваторами
- Побочные действия
- Роль активности холинэстеразы в анестезиологии
- «Контрикал»
- Что такое нейромедиаторы и чем они отличаются от гормонов?
- Когда назначается исследование
- Физико-химические свойства. Токсичность
- 1 Ахэ средства обратимого действия. Их действие длится 2-10 часов физостигмин, прозерин, галантамин и др.
- Заключение
Холинэстераза
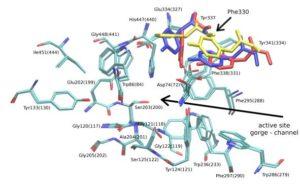
Холинэстеразы — ферменты класса гидролаз, расщепляющие различные эфиры холина с образованием холина и соответствующих кислот.
В крови человека различают два типа фермента: “истинную” или ацетилхолинэстеразу (ацетилгидролаза ацетилхолина, АХЭ, КФ 3.1.1.7) и “ложную” холинэстеразу (ацилгидролаза ацилхолина, ХЭ, КФ 3.1.1.8).
Ферменты различаются по свойствам, локализации, субстратной специфичности.
Ацетилхолинэстераза содержится преимущественно в эритроцитах, также ее активность достаточно высока в нервной и мышечной ткани. Для сыворотки, печени, поджелудочной железы характерен второй тип холинэстеразы.
Ацетилхолинэстераза обладает абсолютной субстратной специфичностью — ее субстратом является только ацетилхолин, в то же время холинэстеразе свойственна абсолютная групповая субстратная специфичность — она расщепляет, кроме ацетилхолина, такие субстраты как бензоилхолин, сукцинилхолин, бутирилхолин и другие эфиры холина.
Холинэстераза синтезируется в печени, представляет собой высокомолекулярный белок (ММ около 300 тыс Д), связанный с альбуминовой фракцией, ее уровень в сыворотке коррелирует с содержанием альбуминов.
Для изучения активности холинэстеразы используют различные способы:
А. Биологические, заключающиеся в обработке исследуемой сывороткой ацетилхолина, после чего им воздействуют на мышцу животного и по степени реакции мышцы судят о количестве ацетилхолина, разрушенного ацетилхолинэстеразой и об активности фермента.
Б. Химические:
- По количеству уксусной кислоты, образованной в результате ферментативной реакции:
| манометрически учитывают объем углекислого газа, выделившегося из карбонатного буфера под влиянием кислоты; |
| фиксируют сдвиг pH раствора по изменению его окраски в присутствии индикаторов (фенолового красного, бромтимолового синего, гидроксиламина); |
| измеряют количество щелочи, пошедшей на титрование уксусной кислоты. |
- Спектрофотометрическое определение изменения абсорбции света при гидролизе субстратов, например, бензоилхолина с максимумом поглощения 240 нм.
- Определение ферментативной активности: а) по количеству расщепленного ацетилхолина хлорида; б) по накоплению продуктов гидролиза в растворе –– по взаимодействию тиохолина (продукта гидролиза специфических субстратов бутирилтиохолина и ацетилтиохолина) с 5,5’‑дитио‑бис‑2‑нитробензойной кислотой.
- Электрохимические методы:
| кондуктометрия; |
| устанавливают величину pH до и после реакции. |
В качестве унифицированных методов утвержден колориметрический метод с субстратом ацетилхолина хлоридом и индикатором феноловым красным и экспресс‑метод с использованием индикаторной бумаги.
Принцип
Под действием холинэстеразы происходит гидролиз ацетилхолина и подкисление среды выделяющейся уксусной кислотой. Сдвиг pH устанавливается с помощью индикатора фенолового красного.
Нормальные величины
| Сыворотка (указанный метод) | 2700‑5700 МЕ |
| или 160‑340 мкмоль/ч·л | |
| или 45‑95 мкмоль/с·л |
Влияющие факторы
in vivo занижает результаты применение нервно‑мышечных релаксантов, пероральных контрацептивов, тестостерона, рентгеноконтрастных средств.
in vitro уменьшение показателей отмечается в присутствии третичных и четвертичных аминов, цитратов, боратов, фторидов, пирофосфатов.
Клинико‑диагностическое значение
Увеличение активности холинэстеразы в крови выявляется при гипертонической болезни, гиперлипопротеинемии IV типа, миоме матки, нефрозе, экссудативной энтеропатии, алкоголизме, сахарном диабете II типа.
Гипоферментемия характерна, как правило, для тяжелых заболеваний печени, отражает вовлечение в процесс паренхимы и снижение синтетической способности гепатоцитов, является прогностическим признаком, так как коррелирует с тяжестью и распространенностью поражения: наблюдается при злокачественных новообразованиях, острых и хронических гепатитах, циррозе, застойной печени при сердечной недостаточности. Кроме заболеваний печени, уменьшение активности холинэстеразы выявляется при острых инфекциях, недостаточности питания, анемиях, мышечной дистрофии, хронических заболеваниях почек, у больных с инфарктом миокарда. Отравление фосфоорганическими соединениями, миорелаксантами, инсектицидами также снижает активность фермента в крови.
Вы можете спросить или оставить свое мнение.
ВКонтакте
Download SocComments v1.3
Дефицит ацетилхолина
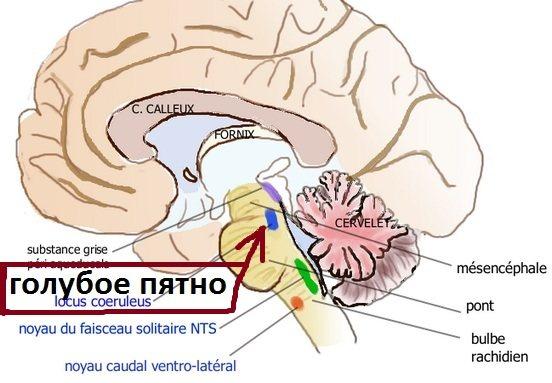
Холинергическая система – часть головного мозга, в которой производится ацетилхолин. По одной из версий, повреждение этой зоны связано с развитием сенильной деменции альцгеймеровского типа. Холинергические эффекты обуславливают старт нейродегенеративных процессов, проявляющихся расстройством кратковременной и долговременной памяти, нарушениями речевой и когнитивных функций, утратой способности ориентироваться в обстановке, невозможностью самообслуживания.
Нехватка ацетилхолина также играет роль в развитии идиопатического синдрома паркинсонизма. Ацетилхолин взаимодействует с нейромедиатором дофамином, обеспечивая плавность движений. Когда существует дисбаланс между ацетилхолином и дофамином, движения человека становятся неточными, возникает:
- ограничение темпа и объема движений;
- непроизвольные быстрые ритмичные колебательные движения в разных частях тела;
- постуральная неустойчивость – невозможность сохранять положение тела;
- отсутствие мышечных реакций на стимулы.
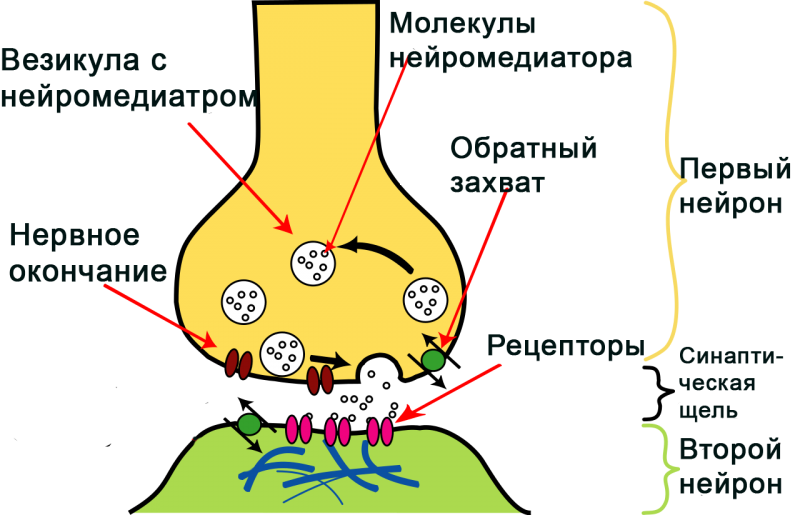
В периферической нервной системе нейромедиатор обеспечивает сокращение сердечной и скелетных мышц. Деструкция ацетилхолиновых рецепторов факторами гуморального и клеточного иммунитета провоцирует развитие миастении – аутоиммунного заболевания, проявляющегося эпизодами мышечной слабости и быстрой утомляемости. Болезнь возникает вследствие аутоиммунной атаки на постсинаптические ацетилхолиновые рецепторы, результатом чего является нарушение нервно-мышечной передачи сигналов. В лечении миастении используют лекарственные вещества, ингибирующие (тормозящие) активность холинэстеразы (фермента, расщепляющего ацетилхолин). Применение этих средств усиливает эффекты ацетилхолина на железы внутренней секреции, сердце, нервные узлы, гладкую и скелетные мышцы.
Доказана роль ацетилхолина в формировании табачной зависимости. Когда никотин достигает структур головного мозга, то активизируются рецепторы ацетилхолина. Со временем мозг привыкает, что никотина, похожего на ацетилхолин, теперь в избытке. Соответственно, раз этого вещества много, то необходимо приспособить процесс синтеза медиаторов к новой реальности. Чтобы это откорректировать, нейроны головного мозга сокращают производство ацетилхолина. Когда собственных запасов ацетилхолина перестает хватать, курильщик будет тянуться к сигарете,чтобы взбодриться, сосредоточиться, успокоиться. То есть у курящего человека функциональные обязанности ацетилхолина переданы никотину.
Историческая справка
Физостигмин, или эзерин, — это алкалоид, получаемый из высушенных зрелых семян физостигмы ядовитой (Physostigma venenosum), называемых калабарскими бобами, орехами эзере, судными орехами и пр. Это многолетнее растение, встречающееся в тропических странах Западной Африки, когда-то использовалось местными племенами для шаманского суда.
В 1840 г. британский военный врач Дэниел привез калабарские бобы в Англию, и их фармакологические свойства были исследованы Кристиосоном (1855), Фрейзером (1863) и Аргайлом Робертсоном (1863). В чистом виде действующий алкалоид был выделен в 1864 г. Иобстом и Гессе, которые и предложили название «физостигмин». В качестве лекарственного средства его впервые использовал в 1877 г. Лакер для лечения глаукомы (основное показание к применению ингибиторов АХЭ и в наше время). Интересные факты из истории изучения физостигмина содержатся в обзорах Karczmar (1970) и Holmstedt (1972).
После того как Стедманом и сотр. была раскрыта связь между структурой физостигмина и его активностью (Stedman, 1929а, Ь), начались исследования ряда других карбаматов, и с 1931 г. стали применять неостигмин для стимуляции перистальтики ЖКТ. Вскоре оказалось, что он оказывает хороший эффект при миастении.
Первое сообщение о синтезе высокотоксичного фосфорорганического ингибитора АХЭ — тетраэтилпирофосфата — было опубликовано Клермоном уже в 1854 г. Самое удивительное в этом сообщении то, что автор вообще смог его опубликовать: он описывает вкус полученного им вещества, а ведь нескольких капель хватило бы для смертельного отравления. Современный этап в исследовании фосфорорганических соединений был открыт сообщением Ланге и Крюгера (1932) о синтезе диметил- и диэтилфторфосфатов. Описанные авторами ощущение удушья и нечеткость зрения, вызываемые этими веществами, видимо, и натолкнули Шрадера на мысль исследовать их инсектицидную активность.
Получив более 2000 соединений, Шрадер определил, какие особенности химической структуры ответственны за инсектицидную активность — и, как выяснилось в дальнейшем, за ингибирование АХЭ (Gallo and Lawryk, 1991). Одно из первых таких соединений — фосфоротиоат паратион — в дальнейшем стало самым распространенным инсектицидом данной группы. Широко применяемый в настоящее время фосфородитиоат малатион также содержит тионфосфорную связь. Непосредственно перед Второй мировой войной и во время нее Шрадер со своими сотрудниками занимался получением боевых отравляющих веществ. При этом в обстановке высокой секретности были получены крайне ядовитые газы — зарин, зоман и табун. Впрочем, в странах антифашистской коалиции также разрабатывались такие вещества, и тоже на основании работ Ланге и Крюгера. В США и Великобритании был лучше всего изучен диизопропилфторфосфат, полученный МакКомби и Саундерсом в 1946 г.
В 1950-х гг. были синтезированы ароматические карбаматы, являющиеся мощными ингибиторами АХЭ и обладающие высокой избирательной токсичностью в отношении насекомых (Ecobichon, 2000).
Взаимодействие холинэстеразы с ингибиторами и реактиваторами
Ингибитор — это вещество, которое снижает активность ферментов (каталитические яды). Ингибиторами холинэстеразы являются некоторые природные и синтетические соединения: фосфорорганические соединения (ФОС), эфиры N-алкилкарбаминовых кислот (карбаматы), четвертичные аммониевые основания, гетероциклические соединения, содержащие третичный или четвертичный атом азота. Некоторые характеристики данных веществ представлены в табл. 1. ФОС и карбаматы иногда называют «полусубстратами» или «плохими субстратами» .
ФОС гидролизуются в активном центре фермента, остаток фосфорила взаимодействует с ОН-группой серина активного центра с образованием «фосфорил-фермента». Следующая стадия катализа — гидролиз «фосфорил-фермента» водой и образование свободного фермента — идет очень медленно, так что активность фермента не восстанавливается. Процесс является необратимым. Активность «фосфорил-фермента» можно восстановить при помощи реактиваторов (например дипироксима) который вытесняет остаток фосфорила из связи холинэстеразы, и молекула фермента освобождается для взаимодействия с субстратом. Фосфорорганические соединения оказывают мощное отравляющее действие на организм. Причиной отравления является накопление негидролизованного ацетилхолина, которое приводит сначала к ускорению проведения нервных импульсов(возбуждение) и далее к блокированию передачи нервных импульсов(паралич). ФОС используют в качестве боевых отравляющих веществ(БОВ), инсектицидов и лекарственных средств.
Карбаматы так же, как и ФОС, гидролизуются в активном центре фермента, отщепленный остаток карбаминовой кислоты взаимодействует с ОН-группой серина с образованием «карбамоил-фермента». Следующая стадия катализа — его гидролиз водой и образование свободного фермента — идет быстрее, чем гидролиз «фосфорил-фермента», но медленнее, чем природных «ацил-ферментов». Активность холинэстеразы блокируется карбаматами на несколько часов и затем восстанавливается. Это обратимый тип ингибирования. Карбаматы широко используются в качестве лекарственных средств для лечения нейродегенеративных заболеваний, при параличах и других болезнях. Описано также масштабное применение физостигмина — обратимого ингибитора холинэстеразы — в качестве профилактического средства от возможного отравления БОВ. В 1991 г. в период войны в Аденском заливе физостигмин был введен 400 тыс. американских солдат с целью скоротечного блокирования (и, следовательно, защиты от инактивации) ацетилхолинэстеразы и холинэстеразы, так как ожидалась атака армии Ирака с использованием нервных газов.
Таблица 1. Ингибиторы холинэстеразы и их действие
| Класс соединений | Тип связи с холинэстеразой | Ингибирование | Препараты |
|---|---|---|---|
| Фосфорорганические соединения | Ковалентная в активном центре | Необратимое | хлорофос, тиофос, армин, зарин, табун |
| Карбаматы | Ковалентная связь в активном центре | Обратимое | физостигмин, карбарил (севин), неостигмин(прозерин), аминокарб |
| Четвертичные аммониевые и гетероциклические соединения | Комплекс с анионным центром фермента | Конкурентное | алкалоиды, галантамин, такрин, донепезил, эдрофония хлорид |
Побочные действия
Антидоты ФОС являются строго рецептурными препаратами. Их не только нельзя принимать без назначения специалиста, но и не следует применять в домашних условиях. Эти лекарства возможно использовать только в условиях стационара под присмотром врача. Они предназачены исключительно для больничного лечения отравления фосфорорганическими веществами.
Оба средства обладают выраженными побочными эффектами. Они могут вызвать падение артериального давления, тахикардию, нарушение функции печени. Может развиться тяжелое состояние, которое называется «холинергическое возбуждение» с беспокойством, бредом и галлюцинациями.
Если человек случайно проглотил фосфорорганическое вещество, то необходимо как можно скорее вызвать врача и оказать пострадавшему первую помощь. Больному промывают желудок раствором марганцовки и дают активированный уголь. Если вещество попало в организм через органы дыхания, нужно вынести человека на свежий воздух и провести промывание носовых ходов. Если яд оказался на коже, то его необходимо смыть водой с мылом.
Дальнейшая помощь будет оказана больному в стационаре, только под наблюдением врача можно провести терапию с использованием антидотов. Это значит, что полностью снять признаки отравления ФОС в домашних условиях невозможно. Нужно помнить, что противоядия эффективны только в первые часы после интоксикации. Чем быстрее будет вызвана скорая медицинская помощь, тем больше шансов на успешное лечение и выздоровление.
Роль активности холинэстеразы в анестезиологии
Необходимость изучения вариантов холинэстеразы возник в середине 1960-х годов. В это время в хирургии стали использовать миорелаксант сукцинилхолин для кратковременной остановки дыхания у пациентов на 3—10 мин. Расчёт проводился на человека с нормальной активностью сывороточной холинэстеразы, но возникли осложнения — если активность холинэстеразы у пациента снижена или отсутствует, то количество миорелаксанта, воздействующее на нервно-мышечное соединение, значительно возрастает и длительность апноэ может составить несколько часов (отмечен случай 9 часового апноэ), что может угрожать жизни больного. При проведении хирургических операций чувствительными к сукцинилхолину оказываются от 4 до 7 % больных. В Дании в 1972 году был создан Исследовательский центр холинэстеразы, в котором к 2000 году обследовались 2300 пациентов из 62 семей.
«Контрикал»
Лекарственное средство, производством которого занимается хорватская фармацевтическая компания «Плива Хрватска д.о.о».
Помимо ингибитора протеолиза, препарат может применяться еще и как сильное гемостатическое средство, потому что он способен останавливать процесс разжижения крови.
Сырьем для производства «Контрикала» служит легочная ткань крупного рогатого скота.
Под действием препарата тормозится выработка не только трипсина, но и плазмина, и калликреина.
Лекарственное средство имеет одну единственную форму выпуска — порошок для приготовления инъекционного раствора, который следует вводить внутривенно.
Стоимость препарата составляет примерно 1500-2000 за 10 флаконов.
Что такое нейромедиаторы и чем они отличаются от гормонов?
Нейромедиаторы (или нейротрасмиттеры) – это химические вещества, осуществляющие передачу сигнала между двумя нервными клетками или между нейронами и другими клетками организма. Они влияют на множество психологических и физиологических функций организма, воздействуют на настроение, память, способность к обучению и концентрацию, регулируют сон, аппетит, от них зависят такие жизненно важные показатели как частота сердечных сокращений, дыхания, особенности пищеварения и пр.
В то же время нейромедиаторы часто путают с гормонами. Это не удивительно, и не только потому, что их регуляторные функции очень схожи: дело в том, что у многих нейромедиаторов есть гормоны-дублеры. Так, есть дофамин-гормон и дофамин-нейромедиатор, есть норадреналин-нейромедиатор и норадреналин-гормон и т.д. Несмотря на то, что у этих веществ одинаковые химические формулы, они оказывают разное воздействие на организм. Основное различие заключается в том, что гормоны вырабатываются только в эндокринных железах, а местом образования нейромедиаторов являются исключительно нейроны. Поэтому и воздействие нейротрансмиттеров ограничивается нервной системой, а гормоны действуют на периферии и не могут проникнуть в мозг – на их пути стоит препятствие в виде гематоэнцефалического барьера.
Различия между гормонами и нейромедиаторами с одинаковой химической формулой можно рассмотреть на примере норадреналина. Норадреналин-гормон вырабатывается в надпочечниках во время стресса, его эффект схож с адреналином, однако он обладает более выраженным сосудосуживающим эффектом и меньше воздействует на частоту сердечных сокращений, оказывает не такое существенное влияние на гладкую мускулатуру кишечника и пр. То есть сферой влияния норадреналина-гормона являются внутренние органы – он участвует в управлении реакции тела на стресс.
В то же время норадреналин-нейромедиатор «царит» в мозге: в стрессовых ситуациях он отвечает за чувство азарта и удовольствия от риска, повышая агрессивность и снижая тревожность. В своей более «мирной» ипостаси он помогает лучше запоминать информацию при обучении.
Когда назначается исследование
Направление на биохимическое исследование крови на холинэстеразу могут дать следующие специалисты:

- невролог;
- гастроэнтеролог;
- гепатолог;
- токсиколог;
- инфекционист.
В качестве предоперационной подготовки анализ крови на холинэстеразу может назначаться анестезиологом либо хирургом.

Исследование может назначаться в следующих случаях:
- людям, работающим в непосредственном контакте с фосфорорганическими веществами (работники сельского хозяйства) либо в химической промышленности;
- в качестве оценки при состоянии острого отравления;
- в качестве предоперационной подготовки, если в анамнезе близких родственников пациента были приступы удушья либо паралича как ответ организма на введение сукцинилхолина.
Определяется активность холинэстеразы в качестве диагностики таких патологий, как:
- гепатит;
- желчекаменная патология;
- холецистит;
- цирроз.
Назначаться исследование может и как показатель адекватности назначенного лечения при печеночных болезнях.
Физико-химические свойства. Токсичность
ФОС – производные
кислот пятивалентного фосфора.
Все ФОС обладают
высокой реакционной способностью.
Особое значение придают реакциям
фосфорилирования, гидролиза и окисления,
поскольку именно эти реакции определяют
стойкость токсикантов в окружающей
среде, имеют отношение к метаболизму и
механизму токсического действия ядов
в организме, на них основаны некоторые
принципы дегазации, обнаружения,
антидотной профилактики и терапии
интоксикаций.
Все ФОС при
взаимодействии с водой подвергаются
гидролизу с образованием нетоксичных
продуктов. Скорость гидролиза ФОС,
растворенных в воде, различна (например,
зарин гидролизуется быстрее, чем зоман,
а зоман – быстрее, чем V-газы).
Зарин– изопропловый эфир метилфторфосфоновой
кислоты представляет собой бесцветную
желтую жидкость со слабым фруктовым
запахом, кипит при температуре 147,3°С.
Максимальная концентрация паров в
воздухе при 20°С составляет 12000 мг/м³,
что способствует его достаточно хорошему
испарению. Стойкость зарина в районе
применения при температуре 20°С и скорости
ветра 2 м/с будет равна 4‑6 часов. В
зимних условиях стойкость возрастает
до 1‑2 суток. Плотность паров по воздуху
– 4,8.
Зарин
хорошо растворим в органических
растворителях, быстро впитывается в
пористые и окрашенные поверхности.
Лучше растворим в жирах, чем в воде.
Однако в воде при 20°С он растворяется
100%. Отсюда следует вывод, что зарин может
проникать в организм всеми путями, в
том числе и через неповрежденную кожу.
В воде,
50% зарина, при рН 7,6 гидролизуется в
течение 300 минут. Значительно гидролиз
ускоряется щелочами. Хлорсодержащие
растворы зарин практически не дегазируют.
Средняя
смертельная доза при действии зарина
ингаляционно составляет 100 мг∙мин/м³,
при действии через кожу смертельная
доза достигает 1500 мг на человека.
Санитарные
потери в свою очередь подразделяются
на поражения легкой степени – 30%, средней
степени –10%, тяжелой и крайне тяжелой
степени – 60%.
Очаг
поражения зариномкак при ингаляционном,
так и при перкутанном воздействии
являютсястойким,
быстрого действия. Ингаляционные
поражения будут ведущими.
Зоман–эфир метилфторфосфоновой кислоты –
прозрачная жидкость со слабым камфорным
запахом. Кипит при температуре 190°С.
Плотность паров по воздуху 6,3. Зоман
хорошо растворим в органических
растворителях и жирах. В воде растворим
плохо (менее 1%). Легко впитывается в
пористые материалы, резиновые изделия.
Гидролиз с водой протекает медленно.
Щелочи и аммиак разрушает зоман быстро,
используются для его дегазации.
Зоман
по своей токсичности превосходит зарин
в 2‑3 раза. Относится
к классу резервныхОВ, пригоден для
оборонительных боевых действий.
Структура
СП идентична зарину. Очаг поражения
зомана как при ингаляционном воздействии,
так и при действии через кожу – стойкий,
быстрого действия.
1 Ахэ средства обратимого действия. Их действие длится 2-10 часов физостигмин, прозерин, галантамин и др.
2)
АХЭ средства необратимого типа действия.
Эти средства очень мощно связываются
с ацетилхолинэстеразой на много дней,
даже месяцев. Однако постепенно, примерно
через 2 недели активность энзима может
восстанавливаться. К ним относятся:
армин, фосфакол и другие антихолинэстеразные
средства из группы фосфорорганических
соединений (инсектициды, фунгициды,
гербициды, БОВ)
эффекты
прозерина
а)
вызывают сужение зрачка (миоз), что
связано с опосредованным возбуждением
М-холинорецепторов круговой мышцы
радужк) и её сокращением;
б)
снижают внутриглазное давление, что
является результатом миоза. Радужка
при этом становится тоньше, в большей
степени раскрываются углы передней
камеры глаза и улучшается отток
внутриглазной жидкости через Фонтановы
пространства и Шлеммов канал.
в)
вызывает спазм аккомодации. стимулирует
М -холинорецепторы ресничной мышцы
имеющей только холинергическую
иннервацию. Сокращение мышцы расслабляет
Циннову связку и, соответственно,
увеличивает кривизну хрусталика.
Хрусталик становится более выпуклым,
а глаз устанавливается на ближнюю точку
видения . прозерин иногда используется
в офтальмологической практике. В этом
плане прозерин показан при открытоугольной
форме глаукомы (0, 5% р-р 1-2 капли 1- 4 раза
в день).
Прозерин
оказывает стимулирующее влияние на
тонус и перистальтику ЖКТ, за счет чего
улучшается продвижение содержимого,
усиливает тонус бронхов (бронхоспазм),
а также тонус и сократительную активность
мочеточников. АХЭ усиливают тонус всех
гладкомышечных органов. прозерин
усиливает секретерную активность желез
внешней секреции (слюнных, бронхиальных,
кишечника, потовых) за счет ацетилхолина.
Прозерин
обычно снижает частоту сокращений
сердца и обладает тенденцией к снижению
АД.
Для
резорбтивного действия назначают (то
есть действия после всасывания)
ПИРИДОСТИГМИН и ОКСАЗИЛ, влияниеие
которых более продолжительно, чем
прозерина. Противопоказания: эпилепсия,
гиперкинезн, бронхиальная астма,
стенокардия, атеросклероз, у больных с
нарушением глотания и дыхания
ФОСФАКОЛ.
Phosphacolum — флаконы по 10 мл 0, 013% и 0, 02%
растворов. Высочайшая токсичность,
поэтому используется только местно в
офтальмологической практике. Отсюда и
показания к применению:
Заключение
Благодаря появлению ингибиторов протеолиза удалось значительно снизить количество смертей от острого панкреатита.
Данные препараты обладают высоким терапевтическим эффектом и способны купировать даже сильные болевые синдромы. Особенно актуально применение ингибиторов протеолиза при панкреатите в острой стадии.
Еще одним достоинством препаратов является небольшое количество побочных эффектов.
Основной недостаток перечисленных выше средств — дороговизна лечения и невозможность постоянного приема. Поэтому применение ингибиторов протеолиза возможно только при острой необходимости.